Cахарный диабет. Патанатомия
Наиболее частой причиной возникновения сахарного диабета
является наследственная неполноценность инсулярного аппарата, а также инфекции (особенно вирусные) и различные стрессорные воздействия. Обязательным фактором в патогенезе этого заболевания является абсолютный или относительный дефицит в организме инсулина, вызывающий нарушение углеводного и других видов обмена. При сахарном диабете главным образом поражается островковый аппарат поджелудочной железы.
В 1901 г. Л. В. Соболев
один из первых произвел тщательное всестороннее морфологическое исследование поджелудочной железы у больных, умерших от .
На вскрытии умерших от диабетической комы при макроскопическом исследовании обычно обнаруживается небольших размеров поджелудочная железа сравнительно плотной консистенции, имеющая на разрезе неравномерное мелкодольчатое строение с признаками отложения жира. При микроскопическом исследовании поджелудочной железы нередко наблюдается атрофия клеток железистых ацинусов, избыточное развитие межуточной соединительной ткани, гиалиноз и склеротические изменения стенок кровеносных сосудов.
Количество островков Лангерганса и их размеры значительно уменьшены, они овальной или неправильной формы и окружены нежной соединительнотканной капсулой. Клетки островкового аппарата в различной степени дистрофически изменены, иногда атрофичны, а в соединительнотканных прослойках отмечается гиалиноз. При некоторых клинических формах сахарного диабета наряду с дистрофическим и атрофическим процессами иногда могут наблюдаться явления регенерации островковой паренхимы.
В настоящее время установлено, что островки Лангерганса человека состоят из трех видов эпителиальных клеток (альфа-, бета- и дельта-клетки). Следует отметить, что дельта-клетки островкового аппарата поджелудочной железы не содержат в своей цитоплазме специфической грануляции и, по-видимому, являются камбиальными элементами, не продуцирующими физиологически активных начал.
Успех в области изучения как количественного, так и качественного состава клеток островков Лангерганса был в значительной степени достигнут благодаря разработанным в последние годы методам гистологической и гистохимической окраски основных клеточных структур. В настоящее время в литературе описано сравнительно много различных методов окраски, используемых для дифференцировки клеток островкового аппарата поджелудочной железы.
Маркировка островковых клеток основана на окрашиваемости в различные цвета их специфической протоплазматической зернистости. С целью дифференцировки альфа- и бета-клеток в настоящее время применяется хромовоквасцовый гематоксилин с флоксипом (по Гомори), модифицированный метод окраски специфической протоплазматической грануляции по способу азан, железный гематоксилин (по Гайденгайну), а также трихромовый метод Массона. Неплохие результаты дает метод импрегнации азотнокислым серебром клеточных элементов островкового аппарата по Грос - Шульцу, а также по Рожеру.
Сравнительно недавно Н. Maske предложил еще один метод, при помощи которого специфическая цитоплазматическая зернистость окрашивается альдегид-фуксипом и железотриоксигематеином; последним реактивом красятся также и ядра островковых клеток. Есть косвенные указания (Р. Уильям), что с помощью флюоресцентной микроскопии можно также дифференцировать островковые клетки поджелудочной железы. Используя указанные методы исследования, было уточнено, что островковые альфа-клетки, продуцирующие в норме глюкагон, или так называемый гипергликемизирующий фактор, обычно крупные, имеют неправильную форму, немногочисленны, содержат в цитоплазме при окраске по Гомори красного цвета зернистость, неаргирофильны и локализуются в периферических частях островка.
Бета-клетки мелкие, преимущественно овальной формы, вырабатывают инсулин, хорошо импрегнируются солями серебра, их значительно больше, чем альфа-клеток; цитоплазма этих клеток нежно зернистая, синеватого оттенка и занимают они центральное положение в островках.
С тех пор, как стало известно , что основные, активно функционирующие клеточные элементы островкового аппарата продуцируют различные гормоны (альфа-клетки - глюкагон, а бета-клетки - инсулин) и по своему воздействию на концентрацию сахара в крови являются антагонистами, наряду с цитологическими исследованиями островковых клеток начали шороко использовать метод подсчета соотношения количества клеточных форм. В нормальных условиях у человека и позвоночных животных в островках Лангерганса количество альфа-клеток по отношению к бета-клеткам обычно составляет 25%, то есть отношение, равное 1: 4.
Однако указанное соотношение в норме значительно варьирует в зависимости от функционального состояния этих клеток. Количественное преобладание того или иного типа клеток свидетельствует о повышении функциональной активности соответствующего вида островковых элементов. Хотя некоторые авторы считают соотношение альфа- и бета-клеток в островках при сахарном диабете но постоянным и не специфичным, большинство исследователей все же полагают, что метод подсчета количественного соотношения клеточных элементов в островках вполне приемлем для микроскопической диагностики.
При выраженных формах сахарного диабета количество бета-клеток обычно снижается, в то время как количество альфа-клеток не изменяется, либо несколько увеличивается. При этом в цитоплазме бета-клеток обнаруживаются признаки дегрануляции, явления дистрофии, а подчас и атрофическио изменения.
История
Диабет сахарный известен с древних времён. О заболевании, протекающем с выделением большого количества мочи, упоминается ещё в папирусе Эберса (примерно 17 век до нашей эры). В 1756 год. Добсон (М. Dobson) обнаружил при этом заболевании в моче сахар, что послужило основанием для существующего названия болезни. Роль поджелудочной железы в патогенезе Диабет сахарный впервые была установлена в 1889 год Мерингом (J. Mehring) и О. Минковским, вызвавшими экспериментальный Диабет сахарный у собак путём удаления поджелудочной железы. Л. В. Соболев в 1901 год показал, что выработка противодиабетического вещества, названного впоследствии инсулином (смотри полный свод знаний), происходит в островках Лангерганса В 1921 год Ф. Бантинг и Бест (Ch. Best), применив методы, рекомендованные Л. В. Соболевым, получили нативный инсулин. Важным этапом в лечении больных сахарным диабетом было введение в клин, практику в середине 20 век пероральных противодиабетических препаратов.
Статистика
Диабет сахарный - распространённое хронический заболевание. В большинстве стран мира встречается у 1-2% населения, в странах Азии - несколько реже. Обычно при активном выявлении на каждого известного больного приходится больной, не знавший о наличии у него этого заболевания. Диабет сахарный в зрелом и пожилом возрасте встречается значительно чаще, чем в детском и юношеском. Во всех странах отмечается прогрессирующее увеличение заболеваемости; в ГДР число больных Диабет сахарный за 10 лет (с 1960 по 1970 год) увеличилось примерно втрое [Шлиак (V. Schliack), 1974].
Широкое распространение, рост заболеваемости, частое развитие сосудистых осложнений ставят Диабет сахарный на уровень ведущих проблем медицины и требуют глубокого его изучения.
Причина смерти больных Диабет сахарный пожилого возраста - поражение сердечно-сосудистой системы, у лиц молодого возраста - почечная недостаточность в результате диабетического гломерулосклероза. В период с 1965 по 1975 год летальность от диабетической комы снизилась с 47,7 до 1,2%; осложнения, связанные с поражением сердечно-сосудистой системы, значительно возросли.
В развитии Диабет сахарный имеет большое значение наследственное предрасположение. Но природа врождённого дефекта и характер наследования при Диабет сахарный точно не установлены. Имеются данные об аутосомно-рецессивном, аутосомно-доминантном путях наследования; допускается возможность многофакторного наследования, при котором предрасположение к Диабет сахарный зависит от сочетания нескольких генов.
Этиология и патогенез
Выявлен ряд факторов, влияющих на развитие Диабет сахарный. Однако из-за большой частоты наследственного предрасположения и невозможности учёта распространения генетического дефекта не удаётся решить, являются эти факторы первичными в развитии Диабет сахарный или они только способствуют проявлению наследственного предрасположения.
Основное в патогенезе Диабет сахарный - относительная или абсолютная инсулинная недостаточность, являющаяся следствием поражения островкового аппарата поджелудочной железы или вызванная внепанкреатическими причинами, приводящая к нарушению различных видов обмена и патологический изменениям в органах и тканях.
Среди факторов, провоцирующих или вызывающих Диабет сахарный, следует указать на инфекционные заболевания, преимущественно у лиц детского и юношеского возраста. Однако специфического поражения инсулинпродуцирующего аппарата при них не установлено. У некоторых людей симптомы Диабет сахарный появляются вскоре после психических и физических травм. Нередко развитию Диабет сахарный предшествует переедание с потреблением большого количества продуктов, богатых углеводами. Нередко Диабет сахарный возникает у больных хроническим панкреатитом (смотри полный свод знаний). Вопрос об этиологической роли атеросклероза артерий, питающих поджелудочную железу, в развитии Диабет сахарный не решён. Диабет сахарный наблюдается чаще у больных гипертонической болезнью, чем у лиц, имеющих нормальное АД.
Установлено, что большее значение в возникновении Диабет сахарный имеет ожирение (смотри полный свод знаний). По данным А. М. Ситниковой, Л. И. Конради (1966), в возрастной группе 45- 49 лет у женщин с избытком веса больше чем на 20% Диабет сахарный отмечается в 10 раз чаще, чем у женщин с нормальным весом тела.У женщин Диабет сахарный может впервые выявляться во время беременности в связи с гормональной перестройкой, усиливающей действие контринсулярных гормонов.
В стадии потенциального диабета нарушения реакции инсулярного аппарата на стимуляцию глюкозой заключаются в более слабом, чем у здоровых, подъёме уровня иммунореактивного инсулина в крови и выявляются только при больших нагрузках глюкозой per os - 200 грамм или внутривенных, особенно при длительном вливании глюкозы.
У больных скрытым Диабет сахарный замедление подъёма уровня иммунореактивного инсулина более выражено, чем у лиц с потенциальным диабетом, и выявляется уже при стандартной пробе на толерантность к глюкозе. В то время как у здоровых после пероральной нагрузки глюкозой пик иммунореактивного инсулина наблюдается через 30-60 минут, у больных скрытым Диабет сахарный он отмечается позднее - через 90-120 минут; по величине он не меньше, чем у здоровых. Однако повышение уровня иммунореактивного инсулина у больных скрытым Диабет сахарный является недостаточным по отношению к подъёму уровня сахара в крови, особенно в течение первого часа после приёма глюкозы.
У больных явным Диабет сахарный инсулярная реакция в ответ на стимуляцию глюкозой снижена во все сроки пробы на толерантность к глюкозе, а при тяжёлой стадии Диабет сахарный с высокими цифрами гипергликемии натощак, наличием ацетонемии (смотри полный свод знаний) и ацидоза (смотри полный свод знаний) инсулярная реакция обычно отсутствует. Наблюдается также снижение уровня иммунореактивного инсулина натощак.
Длительная гипергликемия (смотри полный свод знаний) неизбежно приводит к снижению инсулин-продуцирующей способности островкового аппарата, и течение некомпенсированного Диабет сахарный характеризуется переходом относительной инсулинной недостаточности в абсолютную.
У больных Диабет сахарный с ожирением наблюдаются те же стадии в развитии инсулинной недостаточности, что у больных с нормальным весом: относительная и абсолютная. При ожирении в период, предшествующий появлению инсулинной недостаточности, отмечается резистентность к инсулину, гиперинсулинизм (смотри полный свод знаний) натощак и после нагрузок глюкозой, гипертрофия и гиперплазия р-клеток островков поджелудочной железы. Жировые клетки увеличены в размерах и резистентны к инсулину, что определяется уменьшением числа рецепторов к инсулину. При снижении веса все эти изменения у лиц с ожирением подвергаются обратному развитию. Снижение толерантности к глюкозе при увеличении жировых отложений происходит, очевидно, в связи с тем, что Р-клетки не способны к дальнейшему повышению продукции инсулина для преодоления резистентности к инсулину. Наличие гиперинсулинизма и инсулин-резистентности у лиц с ожирением ещё до нарушения толерантности к глюкозе позволяет считать, что ожирение, по крайнем мере у части больных, является этиологического фактором развития Диабет сахарный Наличие гипертрофии и гиперплазии β-клеток при ожирении, возможно, является причиной более медленного развития абсолютной инсулинной недостаточности при Диабет сахарный, протекающем с ожирением.
Известен ряд гормональных и негормональных антагонистов инсулина, но их первичная роль в развитии инсулинной недостаточности при Диабет сахарный не доказана. Описаны антиинсулинные факторы сыворотки крови, связанные с α и β-липопротеидами, альбуминами. Изучался антагонист инсулина в отношении мышечной ткани, связанный с альбумином - синальбумин. Маловероятно, что антиинсулинные факторы имеют значение в развитии инсулинной недостаточности, так как на стадии потенциального Диабет сахарный не установлено инсулин-резистентности и гиперинсулинизма, которые должны были бы иметь место при наличии антагонизма К инсулину (смотри полный свод знаний).
Известно, что свободные жирные к-ты препятствуют действию инсулина на мышечную ткань. Их уровень в крови повышен при Диабет сахарный. Но это повышение является следствием инсулинной недостаточности, так как устраняется при достижении нормогликемии.
При Диабет сахарный не отмечено нарушения превращений проинсулина в инсулин; инактивация инсулина не ускорена по сравнению со здоровыми лицами. Не получила убедительного подтверждения выдвинутая Антониадисом (Н. N. Antoniades, 1965) гипотеза о повышенном связывании инсулина белками сыворотки крови. Нет также бесспорных данных о развитии аутоиммунного процесса как причины формирования инсулинной недостаточности.
Инсулин - анаболический гормон, способствующий утилизации глюкозы, биосинтезу гликогена, липидов, белков. Он подавляет гликогенолиз, липолиз, глюконеогенез. Первичное место его действия - мембраны инсулин-чувствительных тканей.
При развившейся инсулинной недостаточности, когда снижается или выпадает влияние инсулина, начинают преобладать эффекты гормонов-антагонистов, даже если их концентрация в крови не повышена. При декомпенсированном Диабет сахарный повышается содержание в крови гормона роста, катехоламинов, глюкокортикоидов, глюкагона. Повышение их секреции является реакцией на внутриклеточную недостаточность глюкозы, к-рая имеет место в инсулин-чувствительных тканях при Диабет сахарный Содержание этих гормонов в крови также увеличено при гипогликемии (смотри полный свод знаний). Возникнув как компенсаторная реакция, повышение уровня гормонов-антагонистов в крови приводит к нарастанию диабетических нарушений обмена и инсулин-резистентности.
Антиинсулинный эффект гормона роста связан с увеличением липолиза и повышением уровня свободных жирных кислот в крови, развитием инсулин-резистентности и снижением утилизации глюкозы мышечной тканью. Под действием глюкокортикоидных гормонов (смотри полный свод знаний) усиливается катаболизм белков и глюконеогенез в печени, увеличивается липолиз, снижается захват глюкозы инсулин-чувствительными тканями. Катехоламины (смотри полный свод знаний) подавляют секрецию инсулина, повышают гликогенолиз в печени и мышцах, усиливают липолиз. Антагонистическое по отношению к инсулину действие глюкагона (смотри полный свод знаний) заключается в стимуляции гликогенолиза, липолиза, катаболизма белков.
При инсулинной недостаточности снижено поступление глюкозы в клетки мышечной и жировой тканей, что уменьшает утилизацию глюкозы. Вследствие этого в жировой ткани снижается скорость синтеза свободных жирных кислот и триглицеридов. Наряду с этим происходит усиление процессов липолиза. Свободные жирные к-ты поступают в кровь в большом количестве.
Синтез триглицеридов в жировой ткани при Диабет сахарный снижается, в печени он не нарушен и даже усиливается из-за повышенного поступления свободных жирных кислот. Печень способна фосфорилировать глицерин и образовывать α-глицерофосфат, необходимый для синтеза триглицеридов, в то время как в мышечной и жировой тканях α-глицерофосфат образуется только в результате утилизации глюкозы. Повышение синтеза триглицеридов в печени при Диабет сахарный приводит к их увеличенному поступлению в кровь, а также к жировой инфильтрации печени. Из-за неполного окисления свободных жирных кислот в печени происходит увеличение продукции кетоновых тел (β-оксимасляной, ацетоуксусной кислот, ацетона) и холестерина, что приводит к их накоплению (смотри полный свод знаний Ацетонемия) и вызывает токсическое состояние - так называемый кетоз. В результате накопления кислот нарушается кислотнощелочное равновесие - возникает метаболический ацидоз (смотри полный свод знаний). Это состояние, называемое кетоацидозом, характеризует декомпенсацию обменных нарушений при Диабет сахарный Значительно увеличивается поступление в кровь молочной к-ты из скелетных мышц, селезёнки, стенок кишечника, почек и лёгких (смотри полный свод знаний Лактат-ацидоз). При быстром развитии кетоацидоза организм теряет много воды и солей, что приводит к нарушению водно-электролитного баланса (смотри полный свод знаний Водно-солевой обмен, патология; Минеральный обмен, патология).
При Диабет сахарный нарушается также белковый обмен со снижением синтеза белка и повышением его распада, в связи с чем повышается образование глюкозы из аминокислот (глюконеогенез - смотри полный свод знаний Гликолиз).
Увеличение продукции глюкозы путём глюконеогенеза является одним из основных нарушений обмена в печени при инсулинной недостаточности. Источником образования глюкозы становятся продукты межуточного обмена белков, жиров и углеводов с короткими углеродными цепями. В результате снижения утилизации глюкозы и увеличения её продукции развивается гипергликемия.
Поступление глюкозы в клетки печени, Р-клетки островков поджелудочной железы, хрусталик, нервную ткань, семенные пузырьки, эритроциты, стенку аорты происходит без влияния инсулина и зависит от концентрации глюкозы в крови. Но инсулинная недостаточность приводит к нарушениям обмена и в этих органах и тканях. В результате гипергликемии содержание глюкозы в клетках «инсулиннезависимых» тканей превышает их способность к фосфорилированию и усиливаются процессы её превращения в сорбитол и фруктозу. Увеличение концентрации этих осмотически активных веществ в клетках рассматривается как вероятная причина повреждения тканей, в частности β-клеток, не нуждающихся в инсулине для трансмембранного транспорта глюкозы.
При Диабет сахарный синтез в печени гликопротеидов, в углеводной части которых значительное место занимает глюкоза и образующийся из неё глюкозамин, не нарушен. В результате гипергликемии этот синтез может быть даже ускорен. Нарушению их обмена придаётся значение в развитии диабетической микроангиопатии.
Смотри полный свод знаний также Азотистый обмен, патология; Жировой обмен, патология; Углеводный обмен, патология.
Патологическая анатомия
Морфологически изменения поджелудочной железы (смотри полный свод знаний) отражают функциональную перестройку островкового аппарата (цветной рисунок 7 и 8) и определяют патогенетические механизмы Диабет сахарный Изменения в сосудистой системе организма вторичны, они обусловлены нарушениями обмена, связанными с поражением поджелудочной железы.
Макроскопические изменения поджелудочной железы неспецифичны. Уменьшение объёма и веса органа, липоматоз и цирроз (так называемый гранулярная атрофия) сами по себе не являются доказательством наличия Диабет сахарный, не связаны с прогрессированием заболевания. Изменения, развивающиеся при воспалении, травмах, нарушениях кровообращения, опухолях поджелудочной железы, могут приводить к вторичной инсулинной недостаточности.
Для Диабет сахарный с первичной инсулинной недостаточностью морфологически критерием является нарушение соотношения между аи Р-клетками островков, которые отражают морфологически и функциональный дезорганизацию в системе глюкагон - инсулин, являющуюся основой относительной или абсолютной инсулинной недостаточности.
Соотношение α-клеток и β-клеток, составляющее у здоровых людей от 1:3 до 1:5, может изменяться до 1: 2 или 1:1. Изменение этого индекса может быть связано с уменьшением количества β-клеток (на 7- 10%), что особенно четко выявляется при юношеском Диабет сахарный При этом в сохранившихся β-клетках обнаруживаются признаки гиперплазии и гиперфункции (увеличение митохондрий, просветление матрикса, набухание эргастоплазматического ретикулума, увеличение количества секретируемого инсулина). Одновременно в таких клетках нередко отмечаются признаки альтерации. При юношеском Диабет сахарный часто возникает инфильтрация островков макрофагами и лимфоцитами, приводящая к постепенной гибели β-клеток. Аналогичные изменения наблюдаются в эксперименте при введении животным инсулина. Другая форма дезорганизации островкового аппарата - увеличение количества α-клеток при неизменённом количестве β-клеток. В ответ на это развивается компенсаторная гипертрофия β-клеток, которая также заканчивается функциональным истощением. Гистохимические исследования выявляют уменьшение содержания или исчезновение цинка из цитоплазмы β-клеток.
Относительная или абсолютная недостаточность β-клеток свойственна детской, юношеской и взрослой формам Диабет сахарный, нарастает по мере длительности заболевания, обнаруживая прямую зависимость от его тяжести.
Для Диабет сахарный характерно накопление гликогена в эпителии дистальных канальцев почек (цветной рисунок 5, 6 и 9); в печени гликоген может выявляться не только в цитоплазме, но и в ядрах гепатоцитов и клетках ретикулоэндотелиальной системы, что обычно сопровождается крупнокапельной жировой дистрофией периферических отделов долек (жировая инфильтрация печени).
При Диабет сахарный, продолжающемся 5- 10 лет, возникает генерализованное поражение сосудов - диабетическая ангиопатия, которая представляет собой ответ сосудистого русла на комплекс эндокринных, обменных и тканевых нарушений, свойственных заболеванию, и разделяется на два вида: микроангиопатии и макроангиопатии.
Поражение капилляров и венул состоит в утолщении их базальных мембран, повреждении, пролиферации эндотелия и перицитов и отложении в сосудах гликопротеидных веществ. Микроангиопатия особенно часто развивается в почках, сетчатке глаза (рисунок 1), коже (рисунок 3), мышцах и периневральных пространствах. Иногда она возникает раньше клин, проявлений Диабет сахарный и постепенно прогрессирует. При этом степень выраженности изменений микроциркуляторного русла определяется не столько длительностью Диабет сахарный, сколько степенью его компенсации при лечении. Повреждение, неравномерное утолщение базальных мембран, мукоидное набухание основного вещества сопровождаются нарушением сосудистой проницаемости. В эндотелии выявляется активный пиноцитоз (смотри полный свод знаний), альтерация и десквамация клеток. Реактивные изменения состоят в пролиферации эндотелия и перицитов, накоплении тучных клеток в периваскулярных пространствах. Синтез вещества базальных мембран эндотелием и перицитами, активация синтеза тропоколлагена приводят к необратимым изменениям в виде гиалиноза и склероза сосудов (рисунок 2).
 |
 |  |
Микропрепарат почки при диабетическом гломерулосклерозе: 1 - утолщение базальных мембран капилляров; 2 - отложение ПАС положительных веществ (ПAC реакция; × 200). Рис. 6. Гистотопограмма почки при сахарном диабете: выражены глыбки гликогена (розового цвета); окраска кармином по Бесту; × лупа. Рис. 7 и 8. Микропрепараты поджелудочной железы при сахарном диабете; рисунок 7 -в островке Лангерганса очажки некроза (указаны стрелками); окраска гематоксилин эозином; × 300; рисунок 8 - атрофированные островки Лангерганса (1), компенсаторно гипертрофированный островок (2), липоматоз поджелудочной железы (3); окраска гематоксилин эозином; × 150. Рис. 9. Микропрепарат почки при сахарном диабете: выражены глыбки гликогена (красного цвета) в эпителии и просвете канальцев почки (указаны стрелками); окраска кармином по Бесту. |
||
Важнейшие клинико-морфологические проявления микроангиопатии при Диабет сахарный связаны прежде всего с тяжёлыми поражениями сосудов сетчатки глаза и почек. Поражение сосудов желудочно-кишечного тракта может приводить к хронический гастриту и развитию эрозий слизистой оболочки желудочно-кишечного тракта. Иногда возникает тяжёлая диарея, в основе которой лежит поражение сосудов и нервного аппарата кишечника. Микроангиопатия миокарда приводит к затруднениям коллатерального кровообращения при ангиоспазмах и отягощает прогноз при инфаркте миокарда у больных Диабет сахарный. В артериях среднего калибра может развиваться кальцификация (склероз Макенберга).
Артериолосклероз (смотри полный свод знаний) является обязательным компонентом генерализованного поражения сосудистого русла, но морфологически не имеет существенных отличий от тех видов поражения артериол, которые развиваются при гипертензивной васкулопатии. Наиболее часто поражаются сосуды сетчатки глаза и почек. Артериолы мозга у больных Диабет сахарный поражаются реже, тогда как артериолосклероз в коже и поперечнополосатых мышцах обнаруживается гораздо чаще.
Атеросклероз (смотри полный свод знаний) при Диабет сахарный встречается чаще, развивается раньше и протекает значительно тяжелее, чем обычно. Для атеросклероза при Диабет сахарный свойственна большая степень распространения поражений, которые в сочетании с микроангиопатиями приводят к развитию трофических язв (смотри полный свод знаний) и могут осложниться гангреной (смотри полный свод знаний). Атеросклероз артерий сердца при Диабет сахарный сопровождается нарастанием дисметаболического кардиосклероза (смотри полный свод знаний). Микроскопическая картина, характерная для атеросклероза, дополняется при Диабет сахарный более выраженными изменениями субэндотелиальных и мышечных базальных мембран, большим накоплением гликопротеидов. В очагах липоидной инфильтрации и атероматоза выявляется большое количество фосфолипидов, холестерина и мукополисахаридов.
Несмотря на свойственное Диабет сахарный генерализованное поражение сосудов, в клин, картине заболевания определяется та или иная органная локализация, связанная со степенью поражения сосудов.
Клиническая картина
Потенциальный и скрытый Диабет сахарный являются стадиями, предшествующими клинически выраженному заболеванию.
Потенциальный сахарный диабет протекает без клинической, проявлений. Принято считать, что такой диабет имеется у всех детей, родившихся от больных диабетом родителей. Установлено, что потенциальный Диабет сахарный обнаруживается: а) у лиц с наследственным предрасположением к Диабет сахарный- однояйцовые близнецы больного Диабет сахарный; у лиц, оба родителя которых больны Диабет сахарный; у лиц, один из родителей которых болен Диабет сахарный и имеются больные Диабет сахарный по другой наследственной линии; б) у женщин, родивших живого или мёртвого ребёнка весом 4,5 килограмм и более, а также родивших мёртвого ребёнка с гиперплазией островков Лангерганса при отсутствии у него эритробластоза. Развитие Диабет сахарный примерно у 60-100% людей старше 50 лет, у которых оба родителя или однояйцовый близнец больны Диабет сахарный, позволяет многим исследователям считать, что в период недиагностируемой стадии у них был потенциальный Диабет сахарный Неизвестно, начинается ли эта стадия с момента зачатия или рождения, или развивается в последующие годы жизни, но, несомненно, на этой стадии уже имеются нарушения обмена веществ. Их косвенные показатели - нарушения течения беременности и развития плода у женщин с потенциальным диабетом, гиперплазия островков Лангерганса у плода и другие
Скрытый сахарный диабет. У больных нет никаких клин, признаков. Диабет сахарный выявляется с помощью пробы на толерантность к глюкозе. В этой стадии заболевания содержание сахара в крови натощак и в течение суток нормальное; глюкозурия отсутствует (если нет понижения почечного порога проходимости для сахара). У некоторых больных скрытый Диабет сахарный выявляется только с помощью кортизон (преднизолон) глюкозной пробы.
При скрытом Диабет сахарный у некоторых больных отмечается кожный и генитальный зуд, фурункулёз, пародонтоз. Но у большинства больных в этой стадии заболевания жалобы отсутствуют.
Явный сахарный диабет имеет характерные клин, симптомы: полидипсия (смотри полный свод знаний), полиурия (смотри полный свод знаний), похудание (или ожирение), снижение работоспособности, гипергликемия (смотри полный свод знаний) натощак и в течение дня и гликозурия (смотри полный свод знаний). Выявление ацетонемии (смотри полный свод знаний), ацидоза (смотри полный свод знаний) и ацетонурии (смотри полный свод знаний) указывает на более выраженные диабетические нарушения обмена. Нередко болезнь развивается медленно и постепенно, в других случаях Диабет сахарный начинается бурно и быстро прогрессирует.
Различают три степени тяжести. I степень (лёгкое течение) - отсутствие кетоацидоза, уровень сахара в крови не превышает натощак 140 миллиграмм% (при определении истинной глюкозы). Компенсация (сохранение нормогликемии в течение суток и аглюкозурия, сохранение трудоспособности больного) достигается только диетой, без медикаментозного лечения.
Степень (течение средней тяжести) - гликемия натощак не превышает 220 мг% , а компенсация достигается назначением препаратов сульфанилмочевины или инсулина.
Степень (тяжёлое течение) - гликемия натощак выше 220 миллиграмм%, имеется большая склонность к развитию кетоацидоза, инсулин-резистентности. Часто лабильное течение. Нередко развивается ретинопатия и гломерулосклероз. Такие больные нуждаются в диетотерапии и введении инсулина выше 60, а иногда и выше 120 ЕД в день для достижения компенсации.
Различают два типа Диабет сахарный - юношеский и взрослый. Юношеский Диабет сахарный обычно выявляется в возрасте 15-20 лет, чаще характеризуется острым началом и быстрым прогрессированием, нередко-лабильным течением, во взрослом периоде жизни - развитием ретинопатии и гломерулосклероза. Подкожная жировая клетчатка у больных с юношеским типом часто развита недостаточно, вес тела нормален. Взрослый тип Диабет сахарный выявляется в зрелом или пожилом возрасте, часто сочетается с ожирением, хорошо компенсируется сахароснижающими средствами, применяемыми перорально в сочетании с диетой; протекает более доброкачественно, кетоацидоз развивается редко. Однако часто бывает трудно разграничить эти два типа - Диабет сахарный и в пожилом возрасте может протекать по юношескому типу, а у юношей - по взрослому типу.
Симптомы явного Диабет сахарный у большинства больных развиваются постепенно. Больные вначале их не замечают и обращаются к врачу лишь через несколько недель и даже месяцев после появления первых признаков болезни.
Характерные симптомы явного Диабет сахарный - жажда, сухость во рту, потеря веса, слабость и полиурия. Количество мочи за сутки может составлять 2-6 литров и больше. Отмечается как повышение аппетита, так и его снижение. Жажда связана с обезвоживанием организма, угнетением функции слюнных желёз, сухостью слизистых оболочек рта и глотки.
При декомпенсированном Диабет сахарный у больных отмечается усиление жажды, полиурия, дегидратация кожи, плохое заживление ран. Больные склонны к гнойничковым и грибковым заболеваниям кожи. Фурункулы и карбункулы представляют опасность в связи с тем, что при гнойных процессах нарастает потребность в инсулине и вследствие этого возможно развитие диабетической комы (смотри полный свод знаний).
К поражениям кожи при Диабет сахарный относится липоидный некробиоз. Он проявляется вначале в виде слегка возвышающихся над кожей образований, не исчезающих при надавливании, умеренно эритематозных, с чешуйчатым шелушением. Поражается главным образом кожа голеней (смотри полный свод знаний Некробиоз липоидный).
В результате нарушения липидного обмена могут развиваться ксантомы, представляющие собой папулы желтоватого цвета, которые возникают обычно на коже предплечий, в области локтей и коленей (смотри полный свод знаний Ксантома). Часто наблюдаются гингивит (смотри полный свод знаний), пародонтоз (смотри полный свод знаний).
У больных с тяжёлыми формами наблюдается рубеоз - гиперемия кожи в области скуловых костей, надбровных дуг, подбородка, что связано с расширением кожных капилляров и артериол.
При длительно декомпенсированном Диабет сахарный повышение процессов распада и снижение синтеза белка приводят к атрофическим изменениям в мышцах. Наблюдается уменьшение их массы, дряблость при пальпации, мышечная слабость и повышенная утомляемость. Мышечная атрофия может быть связана с диабетической полиневропатией, нарушениями кровообращения. У некоторых больных развивается диабетическая амиотрофия (смотри полный свод знаний Атрофия мышечная) - асимметричное поражение мышц тазового пояса, бёдер, реже плечевого пояса. При этом наблюдается истончение отдельных мышечных волокон с одновременным утолщением сарколеммы. Диабетическую амиотрофию связывают с изменениями периферического мотонейрона.
Диабетические нарушения обмена могут приводить к развитию остеопороза (смотри полный свод знаний), остеолиза (смотри полный свод знаний).
У больных Диабет сахарный часто присоединяется туберкулёз лёгких. В период декомпенсации, особенно при диабетической коме, имеется повышенная наклонность к развитию очаговых пневмоний.
Поражение сердечно-сосудистой системы при Диабет сахарный характеризуется прогрессирующим развитием атеросклероза крупных артерий и специфическими изменениями мелких сосудов - микроангиопатией. Клинические проявления атеросклероза у больных Диабет сахарный аналогичны проявлениям атеросклероза у больных, не страдающих Диабет сахарный Особенности состоят лишь в том, что у больных Диабет сахарный атеросклероз развивается, как правило, в более молодом возрасте, быстро прогрессирует, одинаково часто поражает мужчин и женщин. Особенно часто бывает нарушение кровообращения нижних конечностей.
Одним из первых симптомов атеросклероза сосудов нижних конечностей является перемежающаяся хромота.
При прогрессировании процесса появляются боли в икроножных мышцах, они становятся стойкими, появляются парестезии, похолодание и побледнение стоп. В дальнейшем развивается багрово-цианотичная окраска стопы, чаще всего в области большого пальца и пятки. Пульсация на a. dorsalis pedis, a. tibialis post, и, как правило, на a. poplitea не определяется уже на ранних клин, стадиях нарушения кровообращения, но у некоторых больных при отсутствии пульса на этих артериях трофические нарушения не возникают вследствие развития коллатерального кровообращения. Наиболее тяжёлое проявление атеросклероза артерий нижних конечностей - сухая или влажная гангрена (смотри полный свод знаний).
Относительно часто наблюдается понижение содержания или отсутствие соляной кислоты в желудочном соке. Язвенная болезнь встречается редко. У пожилых больных, особенно страдающих ожирением, нередко наблюдаются воспалительные процессы в желчных путях и в желчном пузыре.
Диарея может быть связана с ахилией, сопутствующим гастроэнтероколитом, неполноценным питанием, с потреблением большого количества овощей, фруктов, жиров, а также с наличием диабетической полиневропатии. При декомпенсированном Диабет сахарный нередко бывает увеличение печени, обусловленное её жировой инфильтрацией. Функциональные пробы печени при этом обычно не нарушены.
Тяжёлое течение Диабет сахарный характеризуется развитием и прогрессированием диабетического гломерулосклероза (смотри полный свод знаний Гломерулосклероз диабетический); наиболее ранним его признаком является небольшая протеинурия (смотри полный свод знаний), могущая оставаться единственным симптомом в течение ряда лет. В дальнейшем развивается картина недостаточности почек с отёками, переходом в уремию (смотри полный свод знаний). Часты острые и хронический воспалительные процессы в мочевыводящих путях. Наряду с обычным течением пиелита наблюдаются стёртые и бессимптомные его формы. К более редким поражениям почек при Диабет сахарный относится медуллярный некроз, протекающий с картиной тяжёлого септического состояния, гематурией, сильными болями типа почечной колики, нарастающей азотемией.
Наиболее частым и тяжёлым поражением глаз является диабетическая ретинопатия (смотри полный свод знаний), которая клинически проявляется в прогрессирующем снижении зрения с развитием полной слепоты. Кроме того, могут наблюдаться транзиторное изменение рефракции, слабость аккомодации, депигментация радужной оболочки. Отмечается более быстрое созревание старческой катаракты (смотри полный свод знаний). В молодом возрасте может развиться метаболическая катаракта, при которой помутнение хрусталика, начинающееся в субкапсулярной области, имеет вид снежных хлопьев. У лиц с Диабет сахарный чаще развивается глаукома (смотри полный свод знаний).
У больных Диабет сахарный в период декомпенсации наблюдается преходящее повышение функции ряда желёз внутренней секреции (увеличение секреции гормона роста, катехоламинов, глюкокортикоидов) с соответствующей лабораторной симптоматикой.
Приблизительно у 10% больных юношеским типом Диабет сахарный, получающих лечение инсулином, наблюдается лабильное течение заболевания. У этих больных периодически отмечается декомпенсация нарушений обмена даже при строгом соблюдении режима питания, имеются колебания гликемии с быстрыми переходами от гипогликемии к гипергликемии. Это чаще наблюдается у больных с нормальным весом, длительно болеющих, с началом заболевания в детском и молодом возрасте. Считают, что в основе лабильности лежит полная зависимость больных от вводимого инсулина, концентрация которого в крови изменяется медленно и не соответствует изменениям гликемии (инсулинозависимая форма).
Недостаточно адекватное лечение, физическое и психическое перенапряжение, инфекционные болезни, гнойное воспаление могут быстро ухудшить течение Диабет сахарный, привести к декомпенсации и прекоматозному состоянию. Появляется резкая слабость, сильная жажда, полиурия, похудание; кожа сухая, дряблая, видимые слизистые оболочки сухие, резкий запах ацетона изо рта. Речь замедленная, невнятная. Больные ходят с трудом, нетрудоспособны; сознание сохранено. Содержание сахара в крови натощак обычно превышает 300 миллиграмм%. Такое состояние в клин, практике называют также диабетическим кетоацидозом. Если не приняты срочные лечебные меры, развивается диабетическая кома (смотри полный свод знаний). При лабильном Диабет сахарный может развиться и гипогликемическая кома (смотри полный свод знаний Гипогликемия).
У некоторых больных отмечается инсулинрезистентность, под которой обычно понимают потребность в инсулине, превышающую 120 ЕД в сутки, для достижения компенсации. Инсулинрезистентность наблюдается у больных в состоянии диабетического кетоацидоза и комы.
Причины инсулинрезистентности у большинства больных не ясны. Она отмечается при ожирении. У части больных инсулинрезистентность можно связать с высоким титром антител к инсулину в крови.
Поражения нервной системы являются составной частью клинической, проявлений диабета. Вместе с тем они могут наблюдаться в начальном периоде (скрытом) болезни и в некоторой мере затушёвывать другие ранние симптомы Диабет сахарный
Из них чаще всего наблюдаются неврастенический синдром и диабетическая полиневропатия, которые встречаются приблизительно у половины больных, особенно у пожилых людей, длительно страдающих Диабет сахарный Клиника неврастенического синдрома (головная боль, нарушение сна, утомляемость, раздражительность) так же, как и синдрома диабетической полиневропатии (боли в конечностях, расстройства кожной чувствительности и другие), не строго специфична. При диабетической неврастении несколько чаще наблюдаются астенические симптомы - вялость, слабость, пониженное настроение, безразличие к окружающему. Вместе с тем преобладание явлений раздражения или заторможенности зависит в большой степени и от преморбидных особенностей личности больного.
Наблюдаются онемение конечностей, парестезии, полиневрит, характеризующийся болями, а при тяжёлой форме - снижением и исчезновением сухожильных рефлексов, могут наступить атрофические изменения в мышцах. Для Диабет сахарный характерны трофические расстройства (сухость и шелушение кожи на стопах и голенях, ломкость ногтей, гипотрихоз). Двигательные нарушения в конечностях отмечаются не часто, с течением времени снижаются или выпадают сухожильные рефлексы; наблюдаются парезы отдельных нервов, например, отводящего, глазодвигательного, лицевого, бедренного.
Синдром острой энцефалопатии может развиться при нарушении режима лечения инсулином. Он проявляется резкой головной болью, беспокойством, общей слабостью, тошнотой, рвотой, сопорозным состоянием, иногда очаговыми симптомами (парез, афазия, гемигипестезия). Мышечный тонус понижен, зрачки узкие. Уровень сахара в крови относительно невысокий, а в цереброспинальной жидкости - повышен и почти равен уровню сахара в крови.
Синдром хронический энцефалопатии развивается обычно у больных с частыми гипергликемическими и гипогликемическими состояниями и комами в анамнезе. Постепенно снижаются память, внимание, работоспособность, в неврологический статусе появляются умеренно выраженные псевдобульбарные расстройства - слезливость, кашель во время еды, речь с носовым оттенком, гиперсаливация, повышение рефлексов орального автоматизма и мышечного тонуса по пластическому типу, патологический рефлексы. Имеются и некоторые особенности течения нарушений мозгового кровообращения при Диабет сахарный: преобладают нетромботические ишемические инсульты (смотри полный свод знаний), кровоизлияния редки, часты длительные сопорозно-коматозные состояния. Иногда расстройства кровообращения представлены своеобразным альтернирующим синдромом: в течение нескольких недель на одной стороне развивается частичный парез глазодвигательных нервов, на противоположной - небольшие пирамидные и чувствительные нарушения. При синдроме миелопатии (смотри полный свод знаний) - ноющие боли и легкие парезы нижних конечностей, мышечные атрофии. Изредка бывают случаи с преимущественным вовлечением задних столбов (pseudotabes diabetica).
Могут иметь место психические расстройства; клиническая картина их весьма разнообразна. Наиболее часты различные астенические состояния, которые в легких случаях проявляются повышенной раздражительностью, слезливостью, навязчивыми страхами, бессонницей, а в более тяжёлых - общей адинамией, сонливостью, апатией, истощаемостью внимания. Снижение трудоспособности различной степени постоянно.
Аффективные нарушения чаще наблюдаются в виде неглубоких тревожных депрессий, иногда с идеями самообвинения. Реже встречается состояние повышенного настроения с оттенком суетливости. Психозы при Диабет сахарный бывают редко. Может возникать состояние острого психомоторного возбуждения на фоне изменённого сознания. Двигательное беспокойство со зрительными и слуховыми галлюцинациями может достигать значительной интенсивности. Состояние возбуждения может принимать волнообразный, прерывистый характер течения. При особо тяжёлых формах Диабет сахарный возможны острые психозы в виде аменции или аментивно-делириозного помрачения сознания.
При сочетании Диабет сахарный с гипертонической болезнью или церебральным атеросклерозом возникают симптомы слабоумия: снижение критики, памяти на фоне благодушного настроения.
Нарушения половой функции у мужчин, больных Диабет сахарный, в возрасте 25-55 лет наблюдаются примерно в 25% случаев. Иногда это бывает первым симптомом Диабет сахарный. Различают острую, или временную, импотенцию и хроническую. Временная импотенция возникает вследствие резких нарушений метаболизма при обострении течения Диабет сахарный и проявляется ослаблением полового влечения. Либидо восстанавливается при эффективном противодиабетическом лечении. Хронический импотенция характеризуется прогрессирующим ослаблением эрекций, реже - преждевременной эякуляцией, снижением либидо и оргазма. Эта форма импотенции не зависит от длительности Диабет сахарный, уровня гипергликемии и возникает обычно как следствие взаимодействия метаболических, иннервационных, сосудистых и гормональных нарушений. Роль метаболических нарушений подтверждается возникновением временной формы импотенции, очень частым нарушением половых функций у больных, перенёсших повторные диабетические и особенно гипогликемические комы. Гипогликемия влияет на спинальные половые центры, что характеризуется исчезновением спонтанных эрекций, а позже ослаблением адекватных эрекций, расстройствами эякуляции. Поражения периферических вегетативных и соматических нервов, иннервирующих половые органы, часто носят характер смешанного полиневрита. У некоторых больных снижена чувствительность кожи головки полового члена, снижен или отсутствует бульбокавернозный рефлекс, обнаруживаются различные признаки висцеральных невропатий, среди которых наиболее закономерны устанавливаемые цистографией нарушения функции мочевого пузыря. Отмечена закономерная связь между выраженностью нефроангиопатий, ретинопатий, снижением проницаемости капилляров кожи, термолабильностыо сосудов конечностей и частотой импотенции. При наличии атеросклероза может возникать облитерация половых артерий, бифуркации аорты. В последнем случае импотенция сочетается с перемежающейся хромотой (синдром Лериша). Из гормональных нарушений иногда обнаруживается недостаточность андрогенной функции яичек, но чаще концентрация тестостерона в плазме и ответ на стимуляцию гонадотропином у больных Диабет сахарный не изменяются. Более закономерно снижение содержания гонадотропинов, что объясняется морфологически изменениями в системе гипоталамус - гипофиз.
Осложнения, могущие привести к летальному исходу, - тяжёлое поражение сердечно-сосудистой системы (наблюдаемое при юношеском типе Диабет сахарный), гломерулосклероз и диабетическая кома, характеризующаяся повышением содержания сахара в крови (более 300 мг%), повышением содержания кетоновых тел в крови (выше 25 миллиграмм%) и ацетонурией; это сопровождается развитием некомпенсированного ацидоза, нарастанием психоневрологический симптомов, потерей сознания - смотри полный свод знаний Кома.
Диагноз
Диагноз Диабет сахарный устанавливают на основании клин, симптомов и лабораторных показателей: жажда, полиурия, похудание, гипергликемия натощак или в течение дня и гликозурия с учётом анамнеза (наличие в семье больных Диабет сахарный либо нарушений в период беременности - рождение крупных плодов более 4,5 килограмм, мертворождения, токсикоз, многоводие). Иногда Диабет сахарный диагностируется окулистом, урологом, гинекологом и другими специалистами.
При обнаружении гликозурии необходимо убедиться, что она обусловлена гипергликемией. Обычно гликозурия появляется при содержании сахара в крови в пределах 150- 160 миллиграмм%. Гликемия натощак у здоровых людей не превышает 100 миллиграмм%, а её колебания в течение суток находятся в пределах 70-140 миллиграмм% по глюкозооксидазному методу. По методу Хагедорна - Йенсена нормальное содержание сахара в крови натощак не превышает 120 миллиграмм%, а его колебания в течение дня составляют 80-160 миллиграмм%. Если содержание сахара в крови натощак и в течение дня незначительно превышает нормальные величины, то для подтверждения диагноза необходимы повторные исследования и проведение пробы на толерантность к глюкозе.
Наиболее распространённой является проба на толерантность к глюкозе с однократным введением глюкозы per os. В течение трёх дней перед взятием пробы исследуемый должен находиться на диете, содержащей 250-300 грамм углеводов. В течение 15 минут до исследования и на протяжении всей пробы на толерантность к глюкозе он должен быть в спокойной обстановке, в удобном положении сидя или лёжа. После взятия крови натощак исследуемому дают выпить глюкозу, растворенную в 250 миллилитров воды, после чего берут кровь через каждые 30 минут в течение 2½-3 час. Стандартной нагрузкой является 50 грамм глюкозы (рекомендации ВОЗ).
Кортизон (преднизолон) глюкозную пробу проводят так же, как обычную, но за 1½ и 2 часа до неё исследуемый принимает кортизон по 50 миллиграмм или преднизолон по 10 мг. Больным с весом более 72,5 килограмм Конн и Фаянс (J. Conn, S. Fajans, 1961) рекомендуют назначать кортизон в дозе 62,5 миллиграмм. Соответственно доза преднизолона должна быть увеличена до 12,5 миллиграмм.
Критерии нормальной и диабетической пробы на толерантность к глюкозе, принятые в СССР, близки к критериям Конна и Фаянса. Проба на толерантность к глюкозе считается диабетической, если уровень сахара в крови, взятой из пальца натощак, более 110 миллиграмм%, через час после приёма глюкозы - более 180 миллиграмм%, через 2 часа - более 130 миллиграмм% (при использовании глюкозооксидазного метода и метода Шомодьи - Нельсона).
Кортизон (преднизолон)-глюкозная проба считается диабетической, если гипергликемический уровень сахара в крови натощак более 110 миллиграмм%, через 1 час после приёма глюкозы - более 200 миллиграмм% , через часа - более 150 миллиграмм%. Особенно убедительно наличие гликемии через 2 часа после приёма глюкозы более 180 миллиграмм%.
При определении сахара в крови методом Хагедорна - Йенсена все показатели на 20 миллиграмм% выше. Если сахар в крови достигает гипергликемического уровня только через 1 или часа после приёма глюкозы, то проба на толерантность к глюкозе расценивается как сомнительная в отношении Диабет сахарный (смотри полный свод знаний Углеводы, методы определения).
Лечение
Основным принципом лечения Диабет сахарный является нормализация нарушенного обмена веществ. Это положение в СССР было выдвинуто В. Г. Барановым в 1926 год и развито в ряде последующих работ. Основными показателями компенсации нарушений обмена являются: нормализация уровня сахара в крови в течение суток и устранение гликозурии.
Лечение направлено на компенсацию нарушенного при Диабет сахарный обмена веществ и восстановление трудоспособности, а также предупреждение сосудистых, офтальмологический, почечных, неврологический и других расстройств.
Лечение больных скрытым Диабет сахарный проводят диетой; при ожирении - диета в сочетании с бигуанидами. Лечение только диетой может быть применено также больным с лёгкой формой явного Диабет сахарный.
Больным с нормальным весом тела в начале лечения назначается диета, богатая белками, с нормальным содержанием жиров и ограничением углеводов (таблица 1).
Эта диета имеет калорийность 2260 килокалорий Она включает 116 грамм белков, 136 грамм жиров, 130 грамм углеводов.
Замена одних продуктов другими может быть произведена с учётом калорийной ценности пищи и содержания в ней углеводов. По количеству углеводов 25 грамм чёрного хлеба примерно эквивалентны 70 грамм картофеля или 15 грамм крупы. Но такие продукты, как рис, манная крупа, изделия из белой муки, содержат быстро-всасываемые углеводы, и замена ими чёрного хлеба нежелательна. Она может производиться при наличии сопутствующих заболеваний желудочно-кишечного тракта. Сахар исключается полностью. Рекомендуется применение сорбита, ксилита в количестве не более 30 грамм в сутки. В случае отклонений от ориентировочной диеты нельзя допускать уменьшения в пище белков, так как это может вызвать отрицательный азотистый баланс и привести к нарушению самочувствия и работоспособности. При назначении диеты следует принимать во внимание характер труда, возраст, пол, вес, рост и другие факторы.
От лечения только диетой необходимо отказаться, если в течение первых 5-7 дней не происходит снижения уровня сахара в крови и содержания сахара в моче и если на протяжении 10 дней лечения не достигается нормализация гликемии и исчезновение сахара в моче. При нормальном уровне сахара в крови натощак, прочно удерживающемся в течение 2-3 недель, можно перейти к тренировочному расширению диеты- добавляют через каждые 5 дней по 25 грамм чёрного хлеба (или 70 грамм картофеля, или 15 грамм крупы). Перед каждой новой прибавкой продуктов, богатых углеводами, необходимо проверять суточную мочу на сахар и определять содержание сахара в крови натощак. Обычно требуется сделать 4-6 таких прибавок в диете. Расширение диеты производится под контролем веса тела - необходимо добиться его стабилизации на уровне, соответствующем в норме росту, полу и возрасту (смотри полный свод знаний Вес тела).
Диета у больных Диабет сахарный с ожирением должна быть низкокалорийной, с ограничением жиров и углеводов. Количество масла уменьшается до 5 грамм в день, чёрного хлеба - менее 100 грамм в день.
Успешность лечения во многом зависит от того, удаётся ли снизить вес. Ввиду того что диета больных Диабет сахарный с ожирением содержит мало растворимых в жирах витаминов, необходимо назначать витамины А и D в количествах, обеспечивающих суточную потребность. Важно, чтобы пища принималась не реже 4 раз в день через равные промежутки времени. Жидкость не ограничивается, если нет показаний к её ограничению.
Если вес тела снижается, то через 1 месяцев можно прибавить 50 грамм чёрного хлеба и 5 грамм масла и при продолжающемся снижении веса сделать ещё две такие прибавки с интервалом в 1 месяцев. После этого состав диеты следует сохранить до получения желаемого снижения веса. В дальнейшем увеличение в диете продуктов, богатых углеводами и жирами, производится под контролем веса больного и анализов крови и мочи на сахар.
При отсутствии показаний к инсулинотерапии у больных Диабет сахарный лёгкой и средней степени тяжести обычно лечение диетой сочетается с применением перорально противодиабетических средств - сахаропонижающих препаратов сульфанилмочевины (смотри полный свод знаний Сульфаниламидные препараты) и бигуанидов (смотри полный свод знаний).
Сахаропонижающие препараты сульфанилмочевины стимулируют (β-клетки, повышают секрецию инсулина и потенцируют его действие. Они неэффективны у больных с тяжёлой формой Диабет сахарный при абсолютной инсулинной недостаточности. Этими препаратами удаётся компенсировать нарушения обмена преимущественно у больных Диабет сахарный, выявленным в возрасте старше 35 лет. При лечении препаратами сульфанилмочевины нормализация гликемии достигается в течение первой недели, но у некоторых больных - через 2 - 3 недель.
Препараты с продолжительностью действия до 12 часов - толбутамид (бутамид), карбутамид (букарбан), цикламид - применяются 2 раза в сутки (обычно в 7-8 и 17-18 часов, за 1 час до еды). Вначале препараты назначают в дозе 1 грамм 2 раза в сутки, затем доза может быть уменьшена до 1 грамм утром и 0,5 грамм вечером, а при сохранении нормальных показателей сахара в крови - до 0,5 грамм утром и 0,5 грамм вечером. Если нет гипогликемических состояний, то эта доза сохраняется в течение года и более.
Препараты с длительностью сахароснижающего действия до суток - хлорпропамид, хлоцикламид - применяют 1 раз в день утром. Они могут быть назначены также в два приёма, но основная часть суточной дозы должна быть принята утром. Эффективные лечебные дозы хлорпропамида, хлоцикламида составляют 0,25-0,5 грамм в день. Хлорпропамид обладает наиболее сильным сахароснижающим действием. Толбутамид действует слабее, но и токсичность его меньше.
При лечении сахаропонижающими препаратами сульфанилмочевины иногда возникают гипогликемические состояния, которые обычно не бывают тяжёлыми. Все сахаропонижающие препараты сульфанилмочевины могут вызывать кожно-аллергические и диспептические нарушения (сыпь, кожный зуд, понижение аппетита, тошноту, рвоту). Изредка они оказывают токсическое действие на костный мозг, печень, почки. При заболеваниях костного мозга, паренхиматозном поражении печени и почек лечение этими препаратами противопоказано. Они противопоказаны также при беременности (проникают через плаценту!), при воспалительных процессах и наличии конкрементов в мочевыводящих путях. Их применение не показано при тяжёлых формах Диабет сахарный с декомпенсацией и истощением.
Лечение сахаропонижающими препаратами сульфанилмочевины следует проводить при ежемесячном контроле состава периферической крови и исследованиях мочи на белок, уробилин и форменные элементы. Если препараты не устраняют гипергликемию и гликозурию, то может быть испробовано их комбинированное применение с бигуанидами. При неэффективности следует перейти к инсулинотерапии.
Развитие нечувствительности к сахаропонижающим препаратам сульфанилмочевины является, как правило, результатом прогрессирования Диабет сахарный
Лечение инсулином показано больным Диабет сахарный с наличием ацетонемии, ацидоза, ацетонурии, упадком питания, с сопутствующими заболеваниями, например, пиелонефритом, пневмонией, карбункулом и другие, при отсутствии достаточного эффекта от лечения диетой и пероральными противодиабетическими препаратами или при противопоказаниях к применению этих препаратов. Если удаётся снизить дозы инсулина до 2-8 ЕД в сутки при сохранении компенсации Диабет сахарный, возможен переход на пероральные препараты.
У взрослых больных при наличии гликемии натощак 250 миллиграмм% и выше целесообразно сразу начинать лечение инсулином, что не исключает возможности перехода в последующем на препараты сульфанилмочевины.
Попытку перехода на лечение препаратами сульфанилмочевины у взрослых больных можно сделать при суточной дозе инсулина до 20 ЕД, а при наличии ожирения и при более высокой дозе. После назначения этих препаратов инсулин сразу не отменяют, а постепенно уменьшают его дозу под контролем анализов крови и мочи на содержание сахара.
Существуют препараты инсулина короткого, средней продолжительности и длительного действия. При лечении должны использоваться в основном препараты пролонгированного действия. Инсулин короткого действия применяется только по специальным показаниям - при выраженном кетоацидозе, коме, экстренных операциях и некоторых других состояниях. Инсулин вводят подкожно, при диабетической коме- также и внутривенно.
Диета при лечении инсулином по составу должна быть полноценной. Примерное содержание продуктов, богатых углеводами: 250- 400 грамм чёрного хлеба, 50-60 грамм крупы, кроме риса и манной, 200-300 грамм картофеля. Сахар исключается. При лечении инсулином больных Диабет сахарный с ожирением калорийность диеты должна быть уменьшена за счёт ограничения углеводов и жиров так же, как при лечении этих больных одной диетой.
У большинства больных сахаропонижающий эффект водного раствора кристаллического инсулина при подкожном введении проявляется через 15-20 минут, достигает максимума через 2 часа, продолжительность действия не более 6 час. Иногда отмечается более длительное действие. Продукты, богатые углеводами, назначают через 1 и 3½ часа после его введения.
Лучшими современными препаратами инсулина длительного действия являются суспензия инсулин-протамина (СИП) и препараты группы инсулин-цинк-суспензии (ИЦС). Действие СИП достигает максимума через 8-12 часов и продолжается 18- 30 часов. СИП близок по действию к зарубежным препаратам - нейтральному протамину Хагедорна (NPH инсулин). Если действие СИП развёртывается несколько замедленно и имеется гипергликемия в первые часы после его введения, то к нему можно добавлять в одном шприце простой инсулин. Если его действия не хватает на сутки, переходят на лечение ИЦС, к-рая представляет собой смесь двух препаратов - ИЦС аморфной (ИЦС-А) и ИЦС кристаллической (ИЦС-К) в соотношении 3: 7. Она аналогична зарубежному инсулину «Lente».
ИЦС-А: действие начинается через 1-I½ часа, продолжается 10- 12 часов, максимальный эффект наблюдается через 5-8 часов. ИЦС-К: действие начинается через 6-8 часов, достигает максимума через 16- 20 часов, продолжается 30-36 часов.
Протамин-цинк-инсулин (ПЦИ) - препарат, содержащий больше протамина, чем предыдущие. Его эффект начинается через 2-4 часа, максимально действует через 6-12 часов, длительность действия 16-20 часов. К нему нередко требуется добавлять простой инсулин (но в другом шприце!). Этот препарат применяется реже.
Пролонгированные препараты инсулина вводят один раз в день, утром. Продукты, богатые углеводами, при их применении распределяются равномерно в течение дня - каждые 4 часа и обязательно перед сном. Дозы инсулина подбирают под контролем исследований сахара в моче в 4 порциях (первая порция - после введения инсулина до 17 часов, вторая порция - с 17 до 23 часов, третья - с 23 до 7 часов утра, четвертая - с 7 до 8 часов), если инсулин вводят в 8 часов, однако возможны и другие варианты. Более точный подбор доз инсулина производится под контролем дневных колебаний сахара в крови.
Препараты инсулина средней продолжительности действия - ИЦС-А, глобулин-инсулин - применяют при Диабет сахарный средней тяжести один раз в день утром, при более тяжёлых формах заболевания могут быть применены 2 раза в день.
Осложнения инсулинотерапии - гипогликемия и аллергические реакции на введение инсулина.
Диабет сахарный не является противопоказанием для хирургических вмешательств, но перед плановыми операциями необходимо добиться компенсации нарушений обмена. Если ранее применяли препараты сульфанилмочевины, то при небольших вмешательствах их не отменяют, а в случае декомпенсации Диабет сахарный к ним добавляют инсулин.
Большие хирургические вмешательства у всех больных Диабет сахарный следует проводить с введением инсулина. Если больной получал инсулин длительного действия, то утром перед операцией вводят половину обычной дозы и капельно внутривенно назначают 5% раствор глюкозы. В дальнейшем под контролем повторных исследований мочи на сахар и ацетон и крови на сахар решают вопрос о дополнительном введении простого инсулина в течение дня и количестве вливаемой глюкозы. При экстренных операциях также могут потребоваться повторные дополнительные инъекции простого инсулина в течение дня. Диету назначают в соответствии с рекомендациями хирурга; разрешают приём легко усваиваемых углеводов. Применение бигуанидов во время хирургических вмешательств и в послеоперационном периоде противопоказано.
Лечение больных при кетоацидозе и в прекоматозном состоянии проводится инсулином, который вводится дробно 3-4 раза в день и более; при этом необходим постоянный контроль за показателями содержания сахара в крови и ацетонурии. Одновременно вводят в вену изотонический раствор хлорида натрия, дают щелочное питье. Диета в этих случаях может быть расширена за счёт углеводов, жиры ограничиваются.
При неврологический расстройствах лечение должно быть направлено прежде всего на компенсацию углеводного обмена. При очаговых поражениях центральная нервная система, как правило, назначают инсулин; при этом содержание сахара в крови должно быть не ниже 140-160 миллиграмм% (по методу Хагедорна - Йенсена). Показано применение кислорода, препаратов анаболических гормонов, кокарбоксилазы, глутаминовой к-ты, рутина, витаминов группы В. При диабетической полиневропатии показана физиотерапия (массаж, ультразвук, электрофорез с новокаином). При хронический энцефалопатии и нарушении мозгового кровообращения назначают эуфиллин, депопадутин, аминалон, препараты клофибрата.
Лечение при психических расстройствах: при астенических и депрессивных синдромах применяют транквилизаторы, при острых психотических состояниях - аминазин.
Комплексное обследование (неврологический, биохимический, урологический, рентгенологическое) позволяет осуществлять патогенетически обоснованную терапию нарушений половой функции у мужчин при Диабет сахарный Необходима тщательная коррекция нарушений углеводного обмена, витаминотерапия (В 1 , В 12) и физиотерапия. Низкий уровень тестостерона плазмы компенсируют назначением андрогенов. При нормальном уровне тестостерона показан хорионический гонадотропин. Препарат рекомендуется также в случаях бесплодия, обусловленного при Диабет сахарный гипосперматогенезом, нарушением обмена фруктозы.
Санаторно-курортное лечение больных Диабет сахарный входит в комплекс терапевтических мероприятий. Больных, получающих инсулин, целесообразно направлять в местные санатории. В СССР больных Диабет сахарный принимают на лечение санатории в Ессентуках, Боржоми, Пятигорске, Трускавце и другие Противопоказано направление больных в санатории в состоянии декомпенсации, особенно при кетоацидозе.
Лечебная физкультура
Специально подобранные физ. упражнения, вовлекая в работу опорно-двигательный аппарат и мышечную систему, повышают окислительные процессы в организме, способствуют усвоению и потреблению глюкозы мышцами, усиливают действие инсулина. При сочетании инсулинотерапии с физ. упражнениями у больных Диабет сахарный наблюдается выраженное снижение сахара в крови. Физ. упражнения, кроме того, благотворно влияют на функциональное состояние центральная нервная система и сердечно-сосудистой системы, повышают сопротивляемость организма, задерживают развитие ожирения и атеросклероза.
При занятиях лечебный физкультурой физических нагрузка должна соответствовать состоянию сердечно-сосудистой системы больного и его субъективной реакции (усталость, снижение работоспособности и другие). При тяжёлой форме Диабет сахарный и истощении лечебный физкультура противопоказана.
Продолжительность занятия лечебный гимнастикой обычно составляет 25- 30 минут. Физических нагрузка должна нарастать постепенно за счёт увеличен пия количества упражнений и их повторяемости, изменения исходных положений (от положения лёжа до положения сидя и стоя). В комплекс физ. упражнений обязательно следует включать несколько дыхательных упражнений.
При большой физической нагрузке может развиться гипогликемическое состояние. При появлении одышки следует прервать упражнения и 30 - 60 секунд медленно походить по комнате.
Физических упражнения, особенно у начинающих, могут иногда вызвать ощущение усталости, мышечные боли, усиление потливости, боли в области сердца. В таких случаях надо снизить нагрузку - каждое движение повторять меньшее число раз и делать перерывы для отдыха. Упражнения лучше выполнять утром и спустя 1 - 1½ часа после полдника.
Лицам, занятым умственным и малоподвижным трудом, полезны утренняя гигиенических гимнастика, хождение пешком на работу и после неё, физкультурные паузы во время работы, умеренный физических труд в саду, по дому, на огороде, пешеходные прогулки.
В условиях санаторно-курортного лечения показаны прогулки по ровной местности, пешеходные экскурсии, игры в бадминтон, городки, волейбол, но не более 30 минут. Непосредственно после физ. нагрузки с целью повышения окислительных процессов, если нет противопоказаний, можно использовать обтирание, душ, кратковременное купание. Разрешается массаж и самомассаж.
Умеренная физических работа оказывает лечебный действие - предупреждает накопление избыточного жира, поддерживает нормальный жизненный тонус и повышает общую сопротивляемость организма.
Прогноз
Для жизни прогноз при Диабет сахарный благоприятный, особенно при раннем выявлении болезни. Однако диету и, в зависимости от формы болезни, назначенное лечение больной должен соблюдать всю жизнь. Своевременное правильное лечение, соблюдение назначенного режима приводят к компенсации нарушений обмена даже при тяжёлой форме болезни, восстанавливается трудоспособность. У отдельных больных достигается стойкая ремиссия с нормализацией толерантности к глюкозе. В запущенных случаях, при отсутствии адекватной терапии, при различных экстремальных состояниях происходит декомпенсация процесса, может развиться диабетическая кома, тяжёлое поражение почек; при юношеском типе Диабет сахарный - гипогликемическая кома, тяжёлое поражение сердечно-сосудистой системы. В этих случаях прогноз для жизни неблагоприятный.
Беременность и нарушение половой функции у женщин при сахарном диабете
До применения инсулинотерапии часто наблюдались атрофические явления в половой системе, в связи с чем, по данным А. М. Гиневича, способность к зачатию сохраняли только 5 из 100 больных Диабет сахарный женщин. При условии рациональной инсулино и диетотерапии подавляющее большинство женщин, больных Диабет сахарный, сохраняет детородную функцию. Исключение, по мнению Кнорре (G. v. Knorre), составляют болевшие детским и юношеским Диабет сахарный, у которых заметно сокращена продолжительность детородного периода.
Свойственная беременности гормональная перестройка, усиливающая действие контринсулярных гормонов, способствует переходу скрыто протекающего диабета сахарного в явный.
Течение Диабет сахарный в первую половину беременности существенно не меняется либо наблюдается снижение потребности в инсулине. Начиная с 24-28-й недель у большинства беременных увеличивается склонность к кетоацидозу, значительно повышается потребность в инсулине. К концу беременности у части больных наблюдается понижение сахара в крови и моче.
Течение Диабет сахарный при родах обусловлено влиянием таких факторов, как эмоциональный стресс, значительная мышечная работа, нарушение диеты, утомление. Поэтому наряду с развитием ацидоза и гипергликемии у рожениц может наблюдаться и падение уровня сахара в крови.
После родов, особенно после кесарева сечения, потребность в инсулине резко падает, затем постепенно поднимается к исходному уровню до беременности. Все это требует тщательного контроля за беременными и проведения адекватной инсулинотерапии.
Влияние Диабет сахарный на течение беременности проявляется повышением частоты поздних токсикозов беременных (смотри полный свод знаний), многоводия (смотри полный свод знаний), пиелонефрита (смотри полный свод знаний), которые трудно поддаются лечению и значительно ухудшают прогноз беременности.
Во время родов при Диабет сахарный часто наблюдается несвоевременное излитие околоплодных вод, слабость родовых сил, асфиксия плода, затруднённое извлечение плечевого пояса. Крупные размеры детей нередко являются причиной повышенного травматизма в родах. Материнская смертность в родах не высокая; из осложнений послеродового периода наиболее часто встречается гипогалактия (смотри полный свод знаний Лактация).
При отсутствии систематического контроля за беременными и лечения Диабет сахарный перинатальная смертность детей высокая. Согласно наблюдениям Давеке (Н. Daweke) перинатальная смертность при тяжёлой диабетической нефропатии составляет до 40%, при пиелонефрите у беременных - до 32,5% , а при многоводии наряду с высокой перинатальной смертностью часто наблюдаются пороки развития.
У детей, рождённых от матерей, больных Диабет сахарный, довольно часто наблюдается отклонение в развитии; дети отличаются крупным размером и могут иметь характерный вид, напоминающий больных с синдромом Иценко - Кушинга, выраженную незрелость функций. У некоторых детей установлены нарушения белкового, углеводного и жирового обменов, обнаруживается билирубинемия, хронический гипоксия; выявляются ателектазы лёгких, ателектатическая пневмония; все это может сочетаться с симптомами внутричерепной травмы. Эти дети, как правило, гипотоничны, со сниженными рефлексами, быстро теряют в весе и медленно его набирают. Они значительно отстают по адаптационным возможностям от здоровых детей того же возраста; нарушение нормальной динамики фаз сна свидетельствует о функциональной незрелости нервной системы.
Частота пороков развития детей, родившихся от больных Диабет сахарный матерей, колеблется в пределах 6,8- 11%. Наиболее часто наблюдаются врождённые пороки сердца, недоразвитие каудального отдела позвоночника и другие
Организация специализированной акушерской помощи больным Диабет сахарный, тщательное наблюдение за беременными, строгая компенсация нарушений обмена позволили снизить количество осложнений беременности и уменьшить неблагоприятное влияние этих нарушений на плод, а также очень значительно снизить перинатальную смертность.
Исследования Карлссона и Кьелльмера (К. Karlsson, J. Kjellmer) показали, что минимальные перинатальная смертность и заболеваемость детей наблюдаются в группе матерей, у которых во время беременности была стойкая компенсация диабета и средний уровень глюкозы в крови не превышал 100 миллиграмм%. Таким образом, для сохранения плода критерии компенсации Диабет сахарный матери во время беременности должны быть значительно более строгими, чем у небеременных.
Лечение беременных, больных Диабет сахарный, и сохранение жизни плода базируются на следующих основных принципах: максимальная компенсация Диабет сахарный, профилактика и лечение осложнений беременности, рациональный выбор времени и метода родоразрешения, тщательное выхаживание новорожденных.
Для лечения больных Диабет сахарный беременных применяют комбинацию препаратов быстродействующего инсулина и инсулина пролонгированного действия. Необходимую дозу инсулина высчитывают в основном по показаниям и в течение суток, так как гликозурические показатели у беременных в связи с изменением порога проходимости почек для глюкозы не всегда отражают истинную гликемию. Применение препаратов сульфанилмочевины во время беременности противопоказано. Диета при Диабет сахарный должна иметь стабильное содержание углеводов. Примерная суточная раскладка: углеводов - 200-250 грамм, белков - 1,5-2,0 грамм, жиров - до 70 грамм на 1 килограмм веса при максимальном насыщении витаминами и липотропными веществами. Адекватная инсулинотерапия, основанная на возможно более частом исследовании гликемических и гликозурических показателей; профилактика осложнений беременности диктует необходимость постоянного наблюдения за больной акушера и эндокринолога в течение всей беременности. Госпитализация обязательна в ранние сроки беременности и за 2-3 недель до родов; амбулаторный контроль в 1-ю половину беременности необходим каждые 2 недель, а во 2-ю - еженедельно.
Вопрос о сроке и методе родов решается в зависимости от состояния матери, плода и акушерской ситуации. Возрастающая к концу беременности частота осложнений и угроза антенатальной гибели плода вынуждают многих акушеров проводить родоразрешение больных Диабет сахарный в 36 недель. Под контролем тестов, определяющих функциональное состояние и зрелость плода, в ряде клиник стремятся приблизить срок родоразрешения к своевременному, чем обеспечивается снижение заболеваемости и смертности детей. Предпочтение отдаётся родоразрешения) через естественные родовые пути, но при наличии акушерских осложнений расширяются показания к кесареву сечению.
Показаниями к досрочному родоразрешению путём стимуляции родовой деятельности или кесареву сечению является развитие или утяжеление диабетической ретинопатии и диабетического гломерулосклероза, тяжёлый токсикоз второй половины беременности, признаки нарушения жизнедеятельности плода. Показанием к досрочному родоразрешению является появление декомпенсации Диабет сахарный, не поддающейся лечению, быстрое прогрессирование диабетической ретинопатии, гломерулосклероза.
Лечение новорожденных проводится по принципам лечения недоношенных детей. В зависимости от показателей гемодинамики и характера метаболических нарушений применяют эффективные реанимационные мероприятия, введение глюкозы в критические сроки, постоянную оксигенацию в сочетании с введением ферментов, улучшающих тканевое дыхание. По показаниям проводят дегидратационную терапию (смотри полный свод знаний), коррекцию нарушений электролитного обмена, противосудорожное и седативное лечение и другие.
Повышенные требования, предъявляемые к обследованию и лечению больных Диабет сахарный женщин и их детей, в полной мере могут быть осуществлены только при чёткой организации специализированной помощи.
Специализированные акушерские отделения являются центрами, концентрирующими всю лечебную, консультативную, методическую и научно-исследовательскую работу, направленную на разработку эффективных мер по охране здоровья больной матери и её ребёнка.
При обращении супругов к врачу с вопросом о возможности беременности необходимо их предупредить о высокой степени риска для ребёнка (мертворождение, пороки развития) и опасности наследственной передачи заболевания. При желании больная Диабет сахарный может прервать беременность, но если она желает сохранить беременность и к этому нет противопоказаний, то должны быть обеспечены все лечебный мероприятия для сохранения жизни и здоровья ребёнка.
Сахарный диабет у детей
Сахарный диабет у детей встречается во всех периодах детского возраста, в том числе в грудном возрасте и в периоде новорожденности, однако с наибольшей частотой заболеваемость диабетом наблюдается в препубертатном возрасте. Среди всех заболеваний у детей Диабет сахарный составляет, по данным М. М. Бубнова, М. И. Мартынова (1963), от 3,8 до 8%.
Этиология и патогенез
В большинстве случаев Диабет сахарный является генетически обусловленным заболеванием. Оценка генетического дефекта осложняется вариабельностью клин, проявлений заболевания. Мутантный ген распространён широко, имеется около 4-5% гомозигот с пенетрантностью гена для женщин около 90% и для мужчин - 70%. Ген Диабет сахарный (d) имеется у 20-25% людей в популяции, общая частота предрасположенных к Диабет сахарный - около 5%. Ок. 20% людей являются гетерозиготами (Dd) по диабетическому гену, 5% - гомозиготами (dd), 75% - здоровыми (DD). Среди гомозигот 0,9% болеют явным Диабет сахарный, 0,8% - скрытым Диабет сахарный, у 3,3% «диабетическая готовность» (предрасположенность) не поддаётся современной диагностике. У детей чаще Диабет сахарный встречается в семьях, страдающих ожирением, гликогенозом, почечным диабетом, муковисцидозом. Иногда Диабет сахарный может развиться в результате панкреатита, травмы, кровоизлияния, а также порока развития тканей - гамартии (смотри полный свод знаний).
Наследование Диабет сахарный как клинической, синдрома может быть аутосомно-рецессивным, полигенным; наблюдается псевдодоминирование признака. При Диабет сахарный существует наследственная передача неполноценности в составе ДНК или повреждение способности информации в кодирующем механизме ДНК.
Развитие заболевания обусловлено влиянием нескольких генов, находящихся в различных локусах и не всегда являющихся «специфическими» в отношении диабета, но их действие под влиянием ряда факторов может суммироваться и вести к появлению диабетического клинической, синдрома. Генетические дефекты, ведущие к развитию Диабет сахарный, могут быть различными. Это нарушения синтеза и выделения инсулина (мутация структурного гена; мутация гена-регулятора, ведущая к сниженному синтезу инсулина; генный дефект, обусловливающий синтез аномального инсулина; дефекты, обусловливающие ненормальное строение мембран β-клеток или дефекты их энергетики), генные дефекты, приводящие к нечувствительности периферических тканей к инсулину, нейтрализация инсулина вследствие мутации гена-регулятора, обусловливающего высокое содержание инсулиновых антагонистов, и другие Наследственная передача генных дефектов происходит различными путями.
Факторами, провоцирующими начало Диабет сахарный у детей, являются инфекционные заболевания, интоксикации, вакцинация, физические и психические травмы, избыточное употребление жиров и углеводов с пищей.
Абсолютная или относительная недостаточность инсулина (смотри полный свод знаний) играет ведущую роль в патогенезе Диабет сахарный у детей. Имеется предположение, что при Диабет сахарный у детей определённое значение имеют контринсулярные факторы аденогипофиза, среди которых первое место отводится соматотропному гормону. Этим, по-видимому, и объясняется ускорение роста у детей в период, предшествующий возникновению заболевания.
Клиническая картина
Различают потенциальный, скрытый и явный Диабет сахарный Заболевание чаще всего выявляется остро, нередко внезапно (с диабетической комы), а иногда атипично (с абдоминальным синдромом или гипогликемией). Анорексия у детей встречается чаще, чем полифагия. Ночное недержание мочи (смотри полный свод знаний) - один из наиболее частых симптомов начала заболевания.
Заболевание характеризуется своеобразным прогрессирующим течением, которое обусловлено постепенным снижением продукции инсулина поджелудочной железой и влиянием контринсулярных факторов при длительном течении заболевания. Характерна особенная лабильность обменных процессов со значительными колебаниями уровня гликемии (от гипогликемии до чрезмерно высокой гипергликемии) с бурно развивающейся декомпенсацией от незначительных провоцирующих факторов. Причина такой лабильности заключается в чрезмерной чувствительности к эндогенному инсулину, снижении гликогена в печени и мышцах (незрелость нервнорегуляторных механизмов углеводного обмена и высокий энергетический уровень процессов в развивающемся детском организме). Дополнительными факторами, способствующими лабильности уровня сахара в крови у детей, являются инсулинотерапия, мышечная работа, различные стресс-ситуации, сопутствующие заболеванию, хронический инфекции и другие
Установление степени декомпенсации метаболических нарушений и определение критериев компенсации при Диабет сахарный у детей прежде всего необходимо для решения вопросов терапевтической тактики. Говоря о декомпенсации или компенсации Диабет сахарный у детей, необходимо иметь в виду совокупность клин, проявлений заболевания и метаболических нарушений.
Компенсация процессов - полное клинической, благополучие больного ребёнка при отсутствии гликозурии или наличии следов сахара в моче, нормальном уровне кетоновых тел и сахара в крови и отсутствии ацетонурии. На фоне обычного двигательного и диетического режима, подобранной дозы инсулина в фазе компенсации не должно быть гипогликемических состояний и резких колебаний гликемии в течение суток. Любые отклонения от указанных критериев должны рассматриваться как декомпенсация.
Соответственно выраженности патофизиологический сдвигов различают три степени декомпенсации.
Декомпенсация I степени (Д 1) характеризуется неустойчивостью гликемии (периодическое повышение уровня сахара в крови натощак до 200 миллиграмм%) и гликозурией (более 30 грамм за сутки), появлением в утренних порциях мочи следов ацетона, умеренным увеличением ночного диуреза, небольшой жаждой. В этой стадии декомпенсации начинается активация симпатоадреналовой системы; увеличение выделения кортикоидных субстанций, что может рассматриваться как проявление общего синдрома адаптации. Инсулинная активность крови при начальном диабете с постепенным развитием декомпенсации снижается незначительно или остается нормальной. I степень Диабет сахарный легко устранима коррекцией диеты или доз инсулина.
Декомпенсация II степени (Д 2): стойкая гипергликемия, значительная гликозурия, ацетонурия, ацетонемия, полиурия, полидипсия, полифагия, синдром нарастающего эксикоза. Компенсированный метаболический ацидоз. Наряду со снижением инсулинной активности крови усиливается влияние контринсулярных эндокринных желёз, гормоны которых углубляют метаболические нарушения и способствуют образованию ингибиторов инсулина и энзимов, увеличивая, таким образом, дефицит инсулина. Компенсаторно-адаптивные механизмы начинают перерастать в патологические.
Декомпенсация III степени (Д 3) характеризуется нарастанием гипергликемии, гликозурии, ацетонемии, снижением стандартного бикарбоната (могут наблюдаться сдвиги pH крови до 7,3); выраженной ацетонурией, запахом ацетона изо рта, полиурией, жаждой, выраженными симптомами обезвоживания, гепатомегалией. На фоне метаболического ацидоза и вторичного дыхательного алкалоза отмечается значительное повышение лёгочной вентиляции за счёт учащения и углубления дыхания.
Инсулинная активность крови падает до следов, увеличивается экскреция с мочой 17-оксикортикостероидов, наблюдаются значительные изменения в спектре экскретируемых с мочой катехоламинов. Отмечается выраженная гиперальдостеронурия, в крови увеличивается содержание свободных и связанных с белком форм 11-гидроксикортикостероидов. Извращаются ритмы экскреции с мочой электролитов, глюкокортикоидов, проминералокортикоидов, альдостерона, катехоламинов.
Декомпенсация III степени может легко перейти в диабетическую кому и поэтому требует неотложной помощи.
Кома I степени (КК 1): сознание временами затемнено, гипорефлексия, шумное дыхание, тахикардия, резкий запах ацетона изо рта, выраженный эксикоз, гипергликемия, ацетонемия, резкий декомпенсированный метаболический ацидоз и вторичный дыхательный алкалоз. Полиурия сменяется олигурией, поэтому наблюдается относительное уменьшение гликозурии при увеличении процентного содержания глюкозы в моче. Повторная рвота. Ацетонурия. Углубляются и становятся парадоксальными механизмы регуляции основных гомеостатических функций, нарастает трансминерализация.
При коме II степени (КК 2) указанные выше симптомы и метаболические нарушения становятся ещё более выраженными: резчайший декомпенсированный ацидоз, клеточный эксикоз, калиевый дефицит, вторичный дыхательный алкалоз и циркуляторные гемодинамические расстройства, арефлексия и полная потеря сознания. Только неотложная терапия может спасти ребёнка.
Некоторые биохимический показатели динамики декомпенсации и комы представлены в таблице 2.
Гипогликемические состояния должны рассматриваться как декомпенсация Диабет сахарный Гипогликемия чаще встречается в начальном, лабильном периоде диабета, при подборе диеты и инсулинотерапии, при повышении дозы инсулина, после голодания или физ. напряжения. Если начальные значения сахара в крови у ребёнка очень высоки и резко падают, то тяжёлые гипогликемические симптомы могут появиться даже при нормальном уровне сахара в крови. Длительные, часто повторяющиеся гипогликемические состояния у детей могут стать причиной церебральных расстройств.
Диабет сахарный у детей протекает тяжело, лёгкие формы и ремиссии наблюдаются редко. При недостаточно тщательном лечении замедляются процессы роста и развития ребёнка, наблюдается увеличение печени, обусловленное накоплением жира и гликогена в печени. В таких случаях, особенно велика склонность к кетозу, и лечение подобных больных затруднено. У детей, больных Диабет сахарный кариес зубов встречается реже, а пародонтоз чаще, чем в среднем у детей.
Липоидный некробиоз кожи в детском возрасте наблюдается чрезвычайно редко. Изменения со стороны сосудов сетчатки глаза у детей длительное время могут носить обратимый характер. Ведущую роль в развитии и прогрессировании сосудистых изменений играет тяжесть течения Диабет сахарный, глубина обменных нарушений. Влияние длительности заболевания на развитие сосудистых поражений выражено неотчётливо и, вероятно, связано с тем, что по мере нарастания давности болезни прогрессирует её тяжесть.
В ранние сроки после начала заболевания у детей изменяется функциональное состояние почек: увеличение клубочковой фильтрации и канальцевой реабсорбции. Функциональные изменения в почках появляются раньше изменений сосудов глаз.
Общий атеросклероз у детей с Диабет сахарный встречается очень редко. Появление артериолосклероза зависит от продолжительности существования Диабет сахарный и поэтому может иметь место и в детском возрасте.
Чаще всего наблюдается диабетическая полиневропатия. Течение полиневрита, расстройств нервной системы довольно упорное, и только с наступлением половой зрелости нередко наступает стойкая ремиссия.
Диагноз
Диагностика Диабет сахарный в детском возрасте не отличается от таковой у взрослых. Если ребёнок поступает в клинику в состоянии комы, то при постановке диагноза необходимо дифференцировать диабетическую кому с энцефалитом, кровоизлиянием в мозг, гипогликемией, тяжёлым эксикозом, с недостаточностью кровообращения, уремической комой. Решающим при этом являются исследования мочи и крови на содержание сахара.
Лечение
Основная цель лечения состоит в достижении продолжительной компенсации с помощью диеты, инсулина и гигиенических режима. Для обеспечения правильного физических развития больных детей назначают полноценную диету соответственно возрасту. Ограничивают лишь сахар и продукты, приготовленные на сахаре (потребность в них покрывается за счёт сахара, содержащегося в молоке и фруктах). Общая суточная калорийность пищи распределяется следующим образом: 60% килокалорий составляют углеводы, 16% - белки, 24% - жиры. Завтрак составляет 30% суточного рациона, обед - 40%, полдник - 10% , ужин - 20%. При выраженной ацетонурии ограничивают количество жиров и увеличивают количество углеводов, назначают липотропные вещества и продукты, их содержащие (нежирный творог, овсяные и рисовые каши и другие), щелочные минеральные воды и тому подобное
Терапию инсулином назначают в том случае, если суточная экскреция глюкозы с мочой превышает 5% от сахарной ценности пищи (содержание в пище всех углеводов и 50% белков). Показанием для инсулинотерапии служит также уровень сахара в крови, превышающий 200 миллиграмм%, не корригируемый диетой, наличие кетоза, дистрофии и сопутствующих заболеваний.
Детям со скрытым диабетом либо с медленно развивающимся заболеванием при малой выраженности клин, симптомов, а также детям в состоянии ремиссии после начального курса лечения инсулином под тщательным клинической, и лабораторным контролем можно рекомендовать приём сахароснижающих препаратов и бигуанидов.
Основные правила назначения инсулинотерапии детям соответствуют таковым у взрослых (контроль за гликемией и гликозурией). У детей с лёгким течением диабета хорошая компенсация обменных процессов может достигаться однократной инъекцией кристаллического инсулина. У детей с длительным течением заболевания прибегают к комбинации обычного инсулина и инсулина пролонгированного действия. При тяжёлом течении диабета (особенно в пубертатном периоде), кроме смеси вышеназванных препаратов, для временной корреляции нарушенного обмена веществ назначают (вечером или в 6 часов утра) небольшую дозу обычного инсулина.
Лечение диабетической комы и кетоацидотического состояния направлено на устранение ацидоза, токсикоза и эксикоза, обусловленных дефицитом инсулина и сдвигами обменных процессов. Терапевтические мероприятия при коме должны быть быстрыми. В состоянии кетоацидоза и комы ребёнку необходимо немедленно начать инсулинотерапию. Начальная доза инсулина у детей, ранее не получавших инсулин, составляет 0,45-0,5 ЕД на 1 килограмм веса, при KK 1 - 0,6 ЕД на 1 килограмм веса, при КК 2 - 0,7-0,8 ЕД на 1 килограмм веса. При коме 1/3 дозы инсулина вводят внутривенно, остальную часть назначенной дозы - внутривенно капельно в течение 2-3 часов. Детям, ранее получавшим инсулин, независимо от его вида, в состоянии комы вводят простой инсулин с учётом ранее введённой дозы инсулина и времени, прошедшего с момента инъекции.
Для борьбы с дегидратацией, кетоацидозом и циркуляторными расстройствами обязательно введение жидкости (внутривенно и энтерально). Вводят внутривенно струйно изотонический раствор хлорида натрия из расчёта 8-10 миллилитров на 1 килограмм веса с добавлением 100-200 миллиграмм кокарбоксилазы, 2 миллилитров 5% раствора аскорбиновой кислоты. Затем налаживают внутривенное капельное введение жидкости в составе: изотонический раствор хлорида натрия, раствор Рингера - Локка, 5% раствор глюкозы в соотношении 1:1:1 (на первые 6 часов); в дальнейшем состав жидкости меняют в сторону увеличения содержания глюкозы и р-ров, содержащих калий. Суточная потребность вводимой внутривенно жидкости на 1 килограмм веса должна составлять при III степени декомпенсации 45-50 миллилитров, при КК 1 - 50- 60 миллилитров, при КК 2 - 60-70 миллилитров. Продолжительность внутривенного введения жидкости должна составлять при III степени декомпенсации до 35 часов, при КК 1 - до 37 часов, при КК 2 - 38-40 часов.
В первые 3-6 часов больным необходимо вводить 4% раствор бикарбоната натрия. Количество бикарбоната вычисляется по формуле Меллемгарда - Сиггарда - Андерсена: 0,3 × × дефицит оснований (в мили-эквивалент/литров) × × вес тела (в килограмм). В очень тяжёлых случаях необходимо несколько раз в день контролировать результаты лечения путём определения pH, дефицита оснований, стандартного бикарбоната. Чтобы увеличить содержание бикарбоната в плазме, следует при декомпенсации III степени в первые 3-6 часов ввести 140- 160 миллилитров, при КК 1 - 180-200 миллилитров, при КК 2 - 210-250 миллилитров 4% раствора бикарбоната натрия.
Темп введения жидкостей следующий: в первые 6 час. - 50% суточного количества, за последующие 6 час.- 25% , в оставшееся время - 25% .
Вторую инъекцию инсулина в количестве ½-2/3 первоначальной дозы делают через 2-3 часа, в дальнейшем инсулин вводят через 3-4 часа. Введение инсулина через 6 часов от начала лечения должно быть обеспечено адекватным количеством глюкозы (2 грамм глюкозы на 1 ЕД инсулина) для профилактики гипогликемии. Потребность в глюкозе за сутки при Д 3 - 170-200 грамм, при КК 1 - 165- 175 грамм, при КК 2 - 155-165 грамм.
Для предупреждения гипокалиемии в процессе выведения больного из состояния комы и III степени декомпенсации капельным введением жидкости и инсулином необходимо начинать лечение препаратами калия не позже 2-го часа от начала терапии, причём 80% необходимого калия должно быть введено в первые 12-15 часов лечения. Суточная потребность в препаратах калия увеличивается по мере нарастания тяжести состояния больных. При III степени декомпенсации она составляет 3,0-3,2 грамм, при КК 1 - 3,5- 3,8 грамм, при КК 2 - 3,8-4,5 грамм.
Для ликвидации гипокалиемии (смотри полный свод знаний) внутривенно вводят 1% раствор хлорида калия и энтерально 5-10% раствор ацетата или хлорида калия. Может быть рекомендовано также введение фосфата калия, так как утеря клеткой фосфатов выражена сильнее, чем потеря хлоридов.
В связи со значительными циркуляторными расстройствами при коме рекомендуется введение 0,05% раствора строфантина (при отсутствии анурии) в возрастной дозе в 10% растворе глюкозы (введение медленное).
При неукротимой рвоте до внутривенного введения жидкостей необходимо сделать промывание желудка и очистительную клизму.
Для профилактики вторичной инфекции (пневмония, флебит и прочее) после выведения из состояния комы назначают антибиотики (парентерально).
В первые сутки пищу ребёнку не дают. После прекращения рвоты и при улучшении состояния рекомендуется сладкий чай, кисель, компот, щелочные минеральные воды, апельсиновый, лимонный, морковный соки. На вторые сутки диету расширяют за счёт введения манной каши, мясного бульона с сухарями, картофельного пюре, протёртого мяса, обезжиренного творога, в последующие дни ограничивают жиры.
В комплексную терапию кетоацидоза и комы входит назначение глутаминовой к-ты (1,5-3,0 грамм в сутки) с целью связывания кетоновых тел и уменьшения ацидоза, липотропных средств и поливитаминов.
Одним из осложнений при неправильной терапии кетоацидоза и комы является поздний гипокалиемический синдром, который наблюдается через 3-4-6 часов после начала инсулинотерапии. Он характеризуется серой бледностью, значительной мышечной гипотонией, расстройством дыхания, изменением ЭКГ (гипокалиемический тип), расстройством сердечной деятельности (цианоз, тахикардия, низкое АД, неощутимый пульс), парезом кишечника и мочевого пузыря (предупреждение и лечение синдрома - смотри полный свод знаний выше).
Дети, больные Диабет сахарный, требуют постоянного диспансерного наблюдения. Врачебный осмотр должен проводиться не реже одного раза в 1 - 2 месяцев с контрольным исследованием уровня сахара и кетоновых тел крови. Исследования мочи на сахар и кетоновые тела необходимо проводить ежедневно, общий анализ мочи - не реже 1 раза в месяц. Наблюдают за общим состоянием, физическим развитием, режимом дня, диетой, инсулинотерапией. Консультация врача-окулиста - один раз в 3-6 месяцев, консультация отоларинголога и других специалистов - по показаниям. Всех детей с Диабет сахарный обследуют на туберкулёз.
Дети с Диабет сахарный должны пользоваться дополнительным выходным днём в неделю или сокращённым учебным днём; они освобождаются от физических труда в школе и, по показаниям, от школьных экзаменов.
Заболевшие Диабет сахарный подлежат обязательной госпитализации для назначения правильного лечения. При удовлетворительном общем состоянии госпитализация детей осуществляется 1-2 раза в год для повторного обследования и коррекции дозы инсулина. Обязательной госпитализации подлежат все дети с диабетической и гипогликемической комой, выраженными симптомами декомпенсации.
Прогноз зависит от своевременности поставленного диагноза. При диспансерном наблюдении, тщательном лечении, соблюдении режима учёбы и отдыха физическое и психическое развитие ребёнка протекает нормально. При тяжёлой форме с декомпенсацией и комой, а также при почечных осложнениях и инфекционных заболеваниях прогноз менее благоприятный.
Профилактика Диабет сахарный заключается в диспансерном наблюдении за детьми из семей, где имеются больные Диабет сахарный Им проводят исследование мочи и крови на сахар, в отдельных случаях - тест на толерантность к глюкозе. При выявлении у детей предрасположенности к Диабет сахарный необходимо обращать внимание на режим питания, избегать перекармливания, особенно углеводами (конфеты, мучные изделия и другие).
Вас категорически не устраивает перспектива безвозвратно исчезнуть из этого мира? Вы не желаете закончить свой жизненный путь в виде омерзительной гниющей органической массы пожираемой копошащимися в ней могильными червями? Вы желаете вернувшись в молодость прожить ещё одну жизнь? Начать всё заново? Исправить совершённые ошибки? Осуществить несбывшиеся мечты? Перейдите по ссылке:
Ключевые слова
САХАРНЫЙ ДИАБЕТ / ВИРУС ПРОСТОГО ГЕРПЕСА / DIABETES MELLITUS / HERPES SIMPLEX VIRUS TYPE IАннотация научной статьи по клинической медицине, автор научной работы - Зубрицкий М. Г., Недзьведь М. К.
Цель исследования: выявление морфологических признаков воспаления в поджелудочной железе с различными типами сахарного диабета (СД). У 50-ти умерших, в заключительном клиническом диагнозе у которых выставлялся сахарный диабет как основное или сопутствующее заболевание, проводилось изучение историй болезней, окраска кусочков поджелудочной железы из головки, тела, хвоста гематоксилин-эозином, по Ван-Гизону, Конго-Рот, ШИК, а также использовался метод иммунофлюоресценции с моноклональными антителами к вирусу простого герпеса (ВПГ) I типа. Гипергликемический синдром при панкреатите, панкреонекрозе часто расценивается как "впервые выявленный" сахарный диабет . Определенную роль в проявлении гипергликемического синдрома, а также в возникновении СД I и II играет ВПГ. У больных с диагнозом СД I, II типа очень часто выраженность воспалительного процесса достаточно велика, особенно при впервые выявленном гипергликемическом синдроме, есть данные об определенной роли ВПГ в возникновении СД, что указывает на необходимость более внимательного проведения дифференциального диагноза при гипергликемическом синдроме.
Похожие темы научных работ по клинической медицине, автор научной работы - Зубрицкий М. Г., Недзьведь М. К.
-
Морфологические изменения в поджелудочной железе при остром герпетическом менингоэнцефалите
2006 / Зубрицкий М. Г. -
Влияние негативных экзогенных факторов на морфофункциональное состояние поджелудочной железы беременных крыс
2014 / Николаева О. В., Ковальцова М. В., Татарко С. В. -
Хронический герпетический менингоэнцефалит, осложнившийся генерализацией процесса с поражением внутренних органов
2006 / Зубрицкий М. Г. -
К вопросу стандартизации патогистологической диагностики сахарного диабета
2010 / Снигур Григорий Леонидович, Смирнов А. В. -
Панкреатогенный сахарный диабет/сахарный диабет типа 3с: современное состояние проблемы
2018 / Руяткина Л.А., Руяткин Д.С. -
Стеатоз поджелудочной железы - «Белое пятно» панкреатологии
2014 / Пиманов С.И. -
Клиническая и морфологическая характеристика метаболических нарушений при сахарном диабете
2007 / Н. М. Турченко, О. А. Голубев -
Сахарный диабет, возникший вследствие билиарного рецидивирующего панкреатита
2011 / Харлашина Елена Александровна, Кононенко Ирина Владимировна, Смирнова Ольга Михайловна, Майоров Александр Юрьевич -
Клинико-морфологические проявления генерализованной герпетической инфекции с поражением внутренних органов
2007 / Зубрицкий М. Г., Лазаревич Н. А., Силяева Н. Ф., Басинский В. А. -
Циркуляция цитомегаловирусных антител у детей с сахарным диабетом i типа
2014 / Сагоян Гарик Барисович
MORPHOLOGICAL SIGNS OF INFLAMMATION PROCESS OF THE PANCREAS IN TYPE I AND II DIABETIS MELLITUS
Aim: to reveal morphological signs of inflammation in pancreas with different types of diabetes mellitus (DM). In the final diagnosis of 50 cases of death there was DM as the main or secondary disease. The cases of diseases were studied, pieces of head, body, tale of pancreas were stained by Hematoxylin and Eosin, Van-Gison, Congo-Red, immunofluorescence with monoclonal antibodies to the 1 st type of herpes simplex virus (HSV-I). Syndrome of the hyperglycemia during the pancreatitis, pancreonecrosis, is usually identified as the firstly revealed DM. HSV-I is playing certain role in developing of hyperglycemic syndrome and DM. Patients with diagnosis DM I and II type very often have signs of inflammatory process, especially in the firstly revealed DM. There are some data proving the role of the HSV-I in developing of DM. This is important in making accurate differential diagnosis in hyperglycemic syndrome.
Текст научной работы на тему «Морфологические признаки воспалительного процесса в поджелудочной железе при сахарном диабете i и II типа»
УДК 616.379-008.64:616.523-022.6
МОРФОЛОГИЧЕСКИЕ ПРИЗНАКИ ВОСПАЛИТЕЛЬНОГО ПРОЦЕССА В ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЕ ПРИ САХАРНОМ
ДИАБЕТЕ I И II ТИПА
М.Г.Зубрицкий, М.К. Недзьведь, д.м.н, профессор Гродненское областное патологоанатомическое бюро, Белорусский государственный медицинский университет
Цель исследования: выявление морфологических признаков воспаления в поджелудочной железе с различными типами сахарного диабета (СД).
У 50-ти умерших, в заключительном клиническом диагнозе у которых выставлялся сахарный диабет как основное или сопутствующее заболевание, проводилось изучение историй болезней, окраска кусочков поджелудочной железы из головки, тела, хвоста гематоксилин-эозином, по Ван-Гизону, Конго-Рот, ШИК, а также использовался метод иммунофлюоресценции с моноклональными антителами к вирусу простого герпеса (ВПГ) I типа.
Гипергликемический синдром при панкреатите, панкреонекрозе часто расценивается как "впервые выявленный" сахарный диабет. Определенную роль в проявлении гипергликемического синдрома, а также в возникновении СД I и II играет ВПГ.
У больных с диагнозом СД I, II типа очень часто выраженность воспалительного процесса достаточно велика, особенно при впервые выявленном гипергликемическом синдроме, есть данные об определенной роли ВПГ в возникновении СД, что указывает на необходимость более внимательного проведения дифференциального диагноза при гипергликемическом синдроме.
Ключевые слова: сахарный диабет, вирус простого герпеса.
Aim: to reveal morphological signs of inflammation in pancreas with different types of diabetes mellitus (DM).
In the final diagnosis of 50 cases of death there was DM as the main or secondary disease. The cases of diseases were studied, pieces of head, body, tale of pancreas were stained by Hematoxylin and Eosin, Van-Gison, Congo-Red, immunofluorescence with monoclonal antibodies to the 1st type of herpes simplex virus (HSV-I).
Syndrome of the hyperglycemia during the pancreatitis, pancreonecrosis, is usually identified as the firstly revealed DM. HSV-I is playing certain role in developing of hyperglycemic syndrome and DM.
Patients with diagnosis DM I and II type very often have signs of inflammatory process, especially in the firstly revealed DM. There are some data proving the role of the HSV-I in developing of DM. This is important in making accurate differential diagnosis in hyperglycemic syndrome.
Key words: diabetes mellitus, herpes simplex virus type I.
Сахарный диабет представляет собой синдром хронической гипергликемии, развивающейся в результате воздействия генетических и экзогенных факторов . Проявления сахарного диабета из-за его сложной и изменчивой природы часто вызывают немалые трудности в определении различных вариантов этой болезни. По сути это не единая болезнь, а синдром, который может быть вызван множеством факторов. Он может явиться результатом внепанкреатической патологии, такой, как гиперплазия или опухоли переднего гипофиза, гипертиреоидизма. В некоторых случаях диабет может развиться в результате хирургического удаления поджелудочной железы или возникнуть вследствие разрушения панкреатических клеток при таких болезнях поджелудочной железы, как ге-мохроматоз, панкреатит, панкреатолитиаз, опухо-
ли поджелудочной железы . Как показали результаты собственного клинико-морфологическо-го исследования, воспалительные изменения в поджелудочной железе очень часто встречаются при различных формах гипергликемического синдрома, что зачастую не соответствует вставленному при жизни диагнозу. Кроме того, выявилось немалое количество случаев, где в поджелудочной железе были обнаружены признаки поражения вирусом простого герпеса (ВПГ).
Материал и методы. В работе произведен клинико-морфологический анализ на основе изучения историй болезней, системного морфологического исследования поджелудочной железы с применением реакции иммунофлюоресценции. Изучен аутопсийный материал, истории болезней и протоколы вскрытий в 50 случаях смерти, где основным 8 -
или сопутствующим заболеванием в заключительном клиническом диагнозе был выставлен сахарный диабет I или II типа, по данным Гродненского областного патологоанатомического бюро за 20012002 гг.
Для гистологического исследования брались кусочки из головки, тела, хвоста поджелудочной железы. После фиксации в 10% растворе нейтрального формалина окраска проводилась гематоксилин-эозином, по Ван-Гизону, Конго-Рот, ШИК, а также использовался метод иммунофлюоресцен-ции с моноклональными антителами к ВПГ-Т Окрашивание осуществляли по общепринятым прописям. Парафиновые блоки для проведения имму-номорфологического исследования отбирали с учетом результатов предварительного гистологического исследования.
Результаты и обсуждение. Инсулинзависи-мый диабет считается генетически запрограммированным аутоиммунным заболеванием , в возникновении которого заметную роль играют вирусы . Давно замечено, что чем в более молодом возрасте впервые проявился сахарный диабет I типа, тем больше шансов, что поджелудочная железа отреагирует заметным уменьшением клеточной массы в островках, содержания и выработки в них инсулина. Чаще всего сахарный диабет I типа развивается в возрасте до 20 лет, но нередко проявляется и вплоть до 40 лет. В эту группу попадает 10-15% всего диабета. Как показали многочисленные исследования, заболеваемость сахарным диабетом I типа через несколько месяцев после перенесения инфекций, вызванных вирусами краснухи, энцефаломиокардита, эпидемического паро-
тита, коксаки, опоясывающего лишая (H.Zoster), реовирусом, встречаются достоверно чаще . Также в пользу влияния инфекций на проявление сахарного диабета I типа говорит сезонный характер заболеваемости с осенними и зимними подьё-мами в обоих полушариях земли . Можно предположить, что в подобных случаях в поджелудочной железе имеются признаки перенесённого или текущего воспалительного процесса. Материал исследования составил 9 наблюдений летальных исходов (4 мужчины и 5 женщин в возрасте от 40 до 78 лет), где основным или сопутствующим диагнозом был выставлен сахарный диабет I типа. В одном случае заболевание было впервые выявлено, в остальных продолжительность течения заболевания колебалась от 5 до 28 лет.
В случае впервые выявленного сахарного диабета I типа больной 64 лет поступил в стационар с жалобами на слабость, сухость во рту. Подобное состояние отмечал у себя в последние три дня, когда появилась сонливость, заторможенность, неадекватность поведения. При поступлении состояние тяжелое, критика к своему состоянию снижена, АД 145/90 мм рт. ст., содержание сахара в крови 38,85 ммоль/л. В стационаре он прожил менее 1 суток, за это время сахар удалось постепенно снизить до 8,32 ммоль/л. На секции у умершего был обнаружен отек головного мозга с вклинением в большое затылочное отверстие и ишемичес-кий инсульт в левом полушарии мозжечка. Масса поджелудочной железы 80 г, значительные участки замещены жировой клетчаткой. При гистологическом исследовании в поджелудочной железе отмечено резкое уменьшение числа и размеров ост-
%< * >. .v Ч! J К - Г J
Рис. 1. Отек, липоматоз, диффузная воспалительная инфильтрация. Окраска гематоксилином и эозином. X 400
Рис. 2. Диффузная лимфоидная инфильтрация в эндо- и экзокринной части паренхимы поджелудочной железы, заметная также в фиброзной и жировой ткани. Окраска гематоксилином и эозином. Х200
Рис. 3. Очаги выраженного меж- и внутридолькового
фиброза, среди которого можно обнаружить «замурованные» в соединительной ткани островки Лангерганса, также с выраженной воспалительной инфильтрацией. Окраска гематоксилином и эозином. X 200
ровков Лангерганса, гиалиноз в окружающей соединительнотканной капсуле. В клетках островко-вого аппарата отмечено очень большое количество герпетических внутриядерных включений II типа.
В 4-х случаях (4,44%), где сахарный диабет I типа был основным диагнозом, смертельный исход наступал в результате развития кетоацидоза, уремии, а также гнойных осложнений. При морфологическом исследовании было отмечено значительное уменьшение массы поджелудочной железы (60-70 г), отечность ее тканей, наличие слабо выраженного воспалительного процесса преимущественно в жировой и фиброзной ткани (рис. 1, 2, 3). В одном из этих случаев в фибробластах, а также в клетках экзо- и эндокринного отделов обнаружены внутриядерные герпетические включения II типа. В головном мозге в астроцитах и клетках олигодендроглии встречались внутриядерные включения II типа, а в отдельных нейронах включения I типа (рис. 4). В случаях, когда заболевание протекало относительно недолго, в поджелудочной железе, как правило, встречались внутриядерные включения I типа.
Случаи, где сахарный диабет I типа был сопутствующим заболеванием, составили 6 наблюдений (6,66%). Смерть наступала от хронической сердечной недостаточности при хронической ишемической болезни сердца, от дыхательной недостаточности при остром общем милиар-ном туберкулезе, от кровотечения из варикозно расширенных вен пищево-
Рис. 4. Отечный островок Лангерганса с внутриядерными включениями 1 типа (стрелки).
Окраска гематоксилином и эозином. X 100
да при мелкоузловом циррозе печени, а также от ишемического инфаркта ствола головного мозга на фоне резко выраженного атеросклероза артерий головного мозга.
Результаты морфологического исследования представлены в таблицах 1 и 2.
В большинстве случаев отмечалось уменьшение числа и размеров островков Лангерганса. Во всех исследованных случаях были обнаружены воспалительные изменения в поджелудочной железе преимущественно в виде лимфоидной, плаз-моцитарной и макрофагальной инфильтрации. Степень выраженности воспаления колебалась от слабой - 3 случая (33,33%), до умеренной - в 4 случаях (44,44%) и выраженной в - 2 случаях (22,22%). Признаки воспаления были обнаружены как в паренхиме железы, так и в жировой и фиброзной ткани.
Таблица 1. Морфологические изменения поджелудочной железы при сахарном диабете I типа (основной клинический диагноз).
Эндокрин- Лим Гер-
Пол Воз- Дли- Фиброз Экзокринная ная часть -фо- пети
раст тель- часть Уменьшение плаз ти-
ность островков -мо- чес-
забо- В/ Меж Кистоз От- Чис Разме- ци- кие
лева- доль доль стоз- ложе- ла ров тар- вкл
ния ко- ко- ное ние ная юче-
вый вый рас- белка ин- ния
шире- в филь
ние строме тра-
прото- ция
Ж 40 22 года + + - + ++ + + -
Ж 43 28 лет +++ ++ - + ++ ++ ++ +
М 64 Впер- +++ ++ ++ ++ +++ +++ + +++
М 65 + ++ + ++ ++ + ++ -
Примечание: -
отсутствие признака; раженность признака;
Слабая выраженность признака; ++ умеренная вы-+++ резкая степень выраженности признака.
Таблица 2. Морфологические изменения поджелудочной железы при сахарном диабете I типа (диабет - сопутствующий диагноз).
Пол Воз- Дли- Фиброз Экзокрин- Эндокринная Лимфо- Гер-
раст тель- ная часть часть плазмо- пети-
но Уменьшение цитарная чес-
сть островков ин- кие
забо- В/до Меж Ки- От- Чис- Разме- фильтра- вклю-
лева- лько доль стоз- ложе ла ров ция чения
ния вый ко- ное же-
вый рас- ние
М 43 5 лет +++ +++ - - +++ +++ ++ +
М 53 Нес- +++ +++ - - +++ +++ ++ ++
Ж 64 Нес- + + - - + + + +
Ж 70 22 ++ +++ + - ++ ++ Гемора- ++
года гический
Ж 78 >10 + + + - +++ ++ Гемора- -
лет гический
Абсолютная инсулиновая недостаточность в этих наблюдениях связана с уменьшением объема эндокринной части. Это уменьшение более выражено в хронических случаях. В некоторых случаях островки вообще было обнаружить крайне сложно. В случаях, когда заболевание протекало относительно недолго, встречались островки больших размеров. При гистологическом исследовании отмечалась атрофия и дегрануляция остро-вковых клеток. При больших сроках течения диабета Р клетки в абсолютном большинстве случаев были обнаружены в очень малых количествах, реже количество их было снижено умеренно, в отдельных случаях Р клетки вообще не определялись. Другие типы клеток (РР-клетки, глюкагон и соматостатин-продуцирующие) сохранялись в обычных количествах. Инсулит встречался относительно редко (3 случая - 33,3%). Его причиной большинство авторов считает вирусные инфекции, проявление аутоиммунных реакций или комбинацию этих факторов. Фиброз островков наблюдался в 100% случаев, вероятнее всего его причиной является коллапс ретикулиновой сети, следующий за воспалением в островках и разрушением Р клеток . Между клетками островков и капиллярами часто обнаруживался аморфный гиалин.
После детального патоморфо-логического исследования в 2-х случаях был диагностирован геморрагический панкреонекроз (22,22%). В одном случае были обнаружены признаки генерализации герпетической инфекции, что выразилось в обнаружении в поджелудочной железе, печени, различных отделах головного мозга большого количества герпетических включений I и II типа, а также подтверждено методом иммуно-флюоресценции, при котором антиген ВПГ выявлен во всех 3-х отделах поджелудочной железы. Вообще герпетические включения были обнаружены в 6 исследованных случаях (66,66%), при этом в 3-х случаях (33,33%) этот признак был выражен умеренно и даже резко.
Сахарный диабет 2 типа является болезнью среднего возраста. Чаще всего он впервые диагностируется путем лабораторных исследований. При нем редко развивается кетоацидоз, среди больных преобладают женщины. Болезнь ассоциируется с ожирением, инсулинорезистентностью . Сахарный диабет 2 типа встречается в 10 раз чаще, чем диабет 1 типа, и составляет 85% всех случаев диабета . Его этиология полностью не установлена. В то же время при генерализованных вирусных инфекциях часто отмечается гипергли-кемический синдром, на основании которого ставится клинический диагноз вновь выявленного сахарного диабета .
Проведено морфологическое исследование 41 наблюдения смерти больных, у которых основным или сопутствующим заболеванием в заключительном клиническом диагнозе был выставлен сахарный диабет 2 типа.
Среди исследованных было 18 мужчин и 23 женщины в возрасте 39-85 лет с продолжительностью течения заболевания от 6 мес. до 15 лет.
Результаты морфологического исследования представлены в таблицах 3 и 4.
В абсолютном большинстве случаев отмечалось резкое уменьшение числа и размеров островков Лангерганса. В 20 наблюдениях (48,8%) после детального морфологического исследования патологоанатомический диагноз был изменен на хронический панкреатит.
Таблица 3. Морфологические изменения в поджелудочной железе при сахарном диабете 2 типа.
пол возраст Фиброз Уменьшение числа островков Уменьшение размеров островков В оспалительные изменения Герпетические включения
Ж 47 ++ +++ +++ + -
Ж 49 ++ +++ ++ + +
М 56 ++ +++ +++ + -
М 60 ++ ++ ++ + +
Ж 62 ++ - - + -
Ж 65 ++ +++ +++ + +
М 69 ++ +++ +++ - -
М 71 ++ ++ ++ + -
М 71 + ++ ++ + +
М 73 + ++ ++ + -
М 75 ++ +++ +++ + +
М 75 + ++ ++ + +
Ж 75 ++ ++ ++ + -
М 76 ++ - - ++ +
М 76 +++ +++ +++ + +
Ж 77 ++ +++ +++ + -
Ж 78 ++ +++ +++ + -
М 81 + +++ + + -
М 81 ++ +++ +++ + -
Примечание: - отсутствие признака; + слабая выраженность признака; ++ умеренная выраженность признака; +++ резкая степень выраженности признака.
Таблица 4. Морфологические изменения в поджелудочной железе при гиперг ликемическом синдроме с преобладанием воспалительных изменений в органе.
Пол возраст фиброз Уменьшение числа островков Уменьшение размеров островков Воспалительные изменения Герпетические включения
М 39 + + + +++ +
М 51 ++ +++ + +++ +
Ж 53 ++ +++ +++ +++ -
Ж 54 ++ ++ ++ ++ -
Ж 57 +++ +++ +++ ++ +
М 62 ++ ++ ++ + +
М 65 +++ + - ++ +
Ж 69 + + + +++ -
Ж 70 + - - +++ -
Ж 71 ++ +++ +++ + -
Ж 73 +++ ++ + ++ -
Ж 73 +++ ++ ++ ++ +
Ж 74 +++ +++ +++ + +
Ж 76 + + + +++ +
Ж 78 ++ ++ ++ ++ -
Ж 78 ++ + + ++ +
М 80 + +++ +++ + +
Ж 81 ++ +++ +++ ++ +
Ж 84 +++ ++ ++ +++ +
Ж 85 ++ ++ ++ ++ +
Примечание: - отсутствие признака; + слабая выраженность признака; ++ умеренная выраженность признака; +++ резкая степень выраженности признака
В этих наблюдениях в поджелудочной железе обнаружена диффузная и очаговая воспалительная инфильтрация, представленная преимущественно лимфоидными клетками, часто с наличием плаз-моцитов и макрофагов.
Как следует из таблицы 4, в случаях хронического панкреатита преобладали женщины - 15 че-
ловек из 20 (75%), мужчин было 5 (25%). Возраст умерших составил от 39 до 85 лет. Развитие внутри- и междоль-кового фиброза было отмечено во всех случаях. В 5 наблюдениях (25%) он был слабо выражен, в 9 случаях (45%) -умеренно выражен, а в 6 наблюдениях (30%) - резко выражен. Число островков Лангерганса было сохранено в 1 случае (5%), в 5 случаях оно было уменьшено незначительно, в 7 случаях (35%) уменьшение количества было выражено умеренно, и в 7 случаях
Резко выражено. Размеры островков были сохранены в 2 случаях (10%), в 6 случаях (30%) уменьшены незначительно, в 6 - умеренно, в 6 -признак был выражен резко. Воспаление было слабо выражено в 4 случаях (20%), умеренно выражено в 9 случаях (45%), и в 7 случаях (35%) -резко выражено. Герпетические включения были отмечены в 13 случаях (65%) (рис. 5).
Как видно из таблицы 3, возраст умерших с верифицированным диагнозом сахарный диабет 2 типа колеблется от 47 до 81 года, 8 из 21 (38,1%) составили женщины. Мужчин было 13 (61,9%). Фиброз в основном был умеренно выражен - у 14 (6,66%), в 6 случаях он был слабо выражен (28,57%), и в 1 случае (4,76%)
Резко выражен. Уменьшение числа островков Лангерганса в 2 случаях (9,52%) не было отмечено, еще в 2 - слабо выражено, у 6 умерших (28,57%)
Умеренно выражено, а у 11 человек (52,38%) -резко выражено. Уменьшение размеров островков Лангерганса в 2 случаях (9,52%) отсутствовало, в 3 (14,29%) было слабо выражено, в 7 (33,33%) -умеренно выражено, а у 9 умерших (45,86%) - признак был резко выражен. Слабо выраженная воспалительная инфильтрация отмечена в 19 случаях
Рис. 5. Герпетические включения 1 типа в островках Лангерганса и в экзокринном отделе поджелудочной железы (стрелки). Окраска гематоксилином и эозином. X 400
(90,48%), в 1 случае (4,76%), воспалительные изменения были умеренными, и также у 1 умершего они полностью отсутствовали. Герпетические включения обнаружены у 10 человек (47,62%).
В 13 из 20 (65%) случаев хронического панкреатита были обнаружены внутриядерные герпетические включения 1 и 2 типа, феномен тутовой ягоды, которые обнаруживались в фибробластах, клетках экзо- и эндокринного отделов поджелудочной железы и нередко даже в лимфоцитах. Наличие вируса простого герпеса 1 подтверждено методом иммунофлюоресценции, при котором во всех 3 отделах поджелудочной железы выявлялся антиген ВПГ. Такие же изменения, но менее выраженные, были отмечены в 10 случаях (47,62%) сахарного диабета 2 типа. Как видно на рисунке 6, при сахарном диабете II типа гораздо чаще, чем при сахарном диабете I типа встречается гиалиноз сосудов разной степени выраженности.
Таким образом, определенную роль в возникновении сахарного диабета 2 типа играет вирус простого герпеса, что проявляется наличием признаков хронического воспалительного процесса в поджелудочной железе и внутриядерных вирусных включений в клетках этого органа.
1. Диагноз «сахарный диабет», выставленный прижизненно, после детального морфологического исследования часто оказывается проявлением ги-пергликемического синдрома, вызванного хроническим панкреатитом, панкреонекрозом.
2. Определенную роль в возникновении сахарного диабета I и II типов играет вирус простого герпеса, что проявляется наличием признаков хронического воспалительного процесса в поджелу-
Рис. 6. Гиалиноз артериол при сахарном диабете II типа. Окраска по Ван-Гизону. X 200
дочной железе и внутриядерных вирусных включений в клетках этого органа.
Литература
1. Балаболкин М.И. Сахарный диабет. - М., 1994. - С. 12-49.
2. Геллер Л И., Грязнова М.В., Пашко М.М., Дифференциальная диагностика первичного и вторичного сахарного диабета у больных панкреатитом. (Врачебное дело) 1991;1. - Киев: Здоровья. - С. 5-7.
3.Недзьведь М.К.,Рогов Ю.И., Фридман М.В. Клинико-морфоло-гическая диагностика генерализованной герпетической инфекции. Метод. рек. - Мн., БелГИУВ. - 1989. - 20 с.
4.Протас И.И., Коломиец А.Г., Коломиец Н.Д., Недзьведь М.К., Дражина С.А., Дубайская Г.П., Гасич Е.Л., Шанько Л.В., Гузов С.А. Герпесвирусные инфекции (Диагностика и лечение) // Сб. науч. ст. - М., 1990. - С. 23-28.
5.De Fronzo R. A. Pathogenesis of type 2 (non-insulin dependent) diabetes mellitus: a balansed overview // Diabetologia. - 1991. -Vol. 34. - Р. 607-619.
6. The Diabetic Pancreas. Edited by Bruno W. Volk and Klaus F.Welmann. 1977. Plenum Press. N. York. Chapter 9: Idiopatic Diabetes. P. 231-261.
7. Hadish R., Hofmann W., Waldhezz R. Myokarditis and Insulitus nach Coxsackie-Virus-Infection // Z. Kardiol. - 1976. - Vol. 65. -P. 849-855.
8. Handwerger BS, Fernandes G., Brown DM. Immune and autoimmune
aspects of diabetes mellitus // Hum Pathol. - 1980. - Vol. 11. - P. 338-352.
9. Lernimark A. Diabet cell antibodies // Diabetic Med. - 1987. - Vol. 4. - P. 285-292.
10.0lefsky J.M. Pathogenesis of insulin resistance and hyperglykemia in non-insulin-dependant diabetes mellitus // Am. J. Med. - 1985.
Vol. 79. - P. 1-7.
11.Rayfield EJ, Yoon JW. Role of viruses in diabetes. In: Cooperstein SJ, Watkins D, eds. The islets of Langerhans. New York // Academic Press. - 1981. - P. 427-451. 12.Secondary Diabetes. The Spectrum of the Diabetic Syndromes. Edited by Stephen Podolsky; M.Vismapathan; 1980, New York. P. 58-63.
13.Spratt LJ. Seasonal increase of diabetes mellitus // N. Engl. J. Med.
1983. - Vol. 308. - P. 775-776.
14.Yoon JW, Tustin M, Onodera T, Notkins AJ. Virus-induced diabetes mellitus: isoliation of virus from the pancreas of child with the encephalomyocarditis virus // N. Engl. J. Med. - 1979. - Vol. 300.
7.1. КЛАССИФИКАЦИЯ САХАРНОГО ДИАБЕТА
Сахарный диабет (СД) - группа обменных заболеваний, характеризующихся гипергликемией вследствие нарушения секреции и/или эффективности действия инсулина. Хроническая гипергликемия, развивающаяся при СД, сопровождается развитием осложнений со стороны многих органов и систем, в первую очередь, со стороны сердца, кровеносных сосудов, глаз, почек и нервов. СД в общей сложности страдают 5-6 % населения. В экономически развитых странах мира каждые 10-15 лет число больных СД возрастает в 2 раза. Ожидаемая продолжительность жизни при СД снижается на 10-15 %.
Причины развития СД широко варьируют. В подавляющем большинстве случаев СД развивается либо вследствие абсолютного дефицита инсулина (сахарный диабет 1 типа - СД-1), либо вследствие снижения чувствительности периферических тканей к инсулину в сочетании с секреторной дисфункцией β-клеток поджелудочной железы (сахарный диабет 2 типа - СД-2). В ряде случаев отнесение пациента к СД-1 или СД-2 затруднено, тем не менее на практике более значима компенсация СД, а не точное установление его типа. Этиологическая классификация выделяет четыре основных клинических класса СД (табл. 7.1).
Наиболее часто встречающиеся СД-1 (п. 7.5), СД-2 (п. 7.6) и гестационный СД (п. 7.9) обсуждаются в отдельных главах. На другие специфические типы приходится всего около 1 % случаев СД. Этиология и патогенез этих типов СД представляется более изученной по сравнению с СД-1 и особенно СД-2. Ряд вариантов СД обусловлено моногенно наследуемыми генетическими дефектами функции β-клеток. Сюда относятся различные варианты аутосомно-доминантно наследуемого синдрома MODY (англ. maturity onset diabetes of the young - диабет взрослого типа у молодых), которые характеризуются нарушением, но не отсутствием секреции инсулина при нормальной чувствительности к нему периферических тканей.
Табл. 7.1. Классификация сахарного диабета
Казуистически редко встречаются генетические дефекты действия инсулина, связанные с мутацией рецептора инсулина (лепречаунизм, синдром Рабсона-Мандехолла). СД закономерно развивается при заболеваниях экзокринной части поджелудочной железы, приводящих к деструкции β-клеток (панкреатит, панкреатэктомия, кистозный фиброз, гемохроматоз), а также при ряде эндокринных заболеваний, при которых происходит избыточная продукция контроинсулярных гормонов (акромегалия, синдром Кушинга). Лекарственные препараты и химикаты (вакор, пентамидин, никотиновая кислота, диазоксид и др.) редко являются причиной СД, но могут способствовать манифестации и декомпенсации заболевания у лиц с инсулинорезистентностью. Ряд инфекционных заболеваний (краснуха, цитомегалия, коксаки- и аденовирусная инфекция) могут сопровождаться деструкцией β-клеток, при этом у большинства пациентов определяются иммуногенетические маркеры СД-1. К редким формам иммуноопосредованного диабета относят СД, развивающийся у пациентов со «stiff-rnan»-синдромом (аутоиммунное неврологическое заболевание), а также СД вследствие воздействия аутоантител к рецепторам инсулина. Различные варианты СД с повышенной частотой встречаются при
многих генетических синдромах, в частности, при синдромах Дауна, Клайнфелтера, Тернера, Вольфрама, Прадера-Вилли и ряде других.
7.2. КЛИНИЧЕСКИЕ АСПЕКТЫ ФИЗИОЛОГИИ УГЛЕВОДНОГО ОБМЕНА
Инсулин синтезируется и секретируется β-клетками островков Лангерганса поджелудочной железы (ПЖЖ). Кроме того, островки Лангерганса секретируют глюкагон (α-клетки), соматостатин (δ-клетки) и панкреатический полипептид (РР-клетки). Гормоны островковых клеток взаимодействуют между собой: глюкагон в норме стимулирует секрецию инсулина, а соматостатин подавляет секрецию инсулина и глюкагона. Молекула инсулина состоит из двух полипептидных цепей (А-цепь - 21 аминокислота; В-цепь - 30 аминокислот) (рис. 7.1). Синтез инсулина начинается с образования препроинсулина, который расщепляется протеазой с образованием проинсулина. В секреторных гранулах аппарата Гольджи проинсулин расщепляется на инсулин и С-пептид, которые высвобождаются в кровь в процессе экзоцитоза (рис. 7.2).
Основным стимулятором секреции инсулина является глюкоза. Высвобождение инсулина в ответ на повышение уровня глюкозы в крови происходит двухфазно (рис. 7.3). Первая, или острая, фаза длится несколько минут, и она связана с высвобождением накопив-
 Рис. 7.1.
Схема первичной структуры молекулы инсулина
Рис. 7.1.
Схема первичной структуры молекулы инсулина
 Рис. 7.2.
Схема биосинтеза инсулина
Рис. 7.2.
Схема биосинтеза инсулина
шегося в β-клетке инсулина в период между приемами пищи. Вторая фаза продолжается до тех пор, пока уровень гликемии не достигнет нормального тощакового (3,3-5,5 ммоль/л). Сходным образом на β- клетку воздействуют препараты сульфонилмочевины.
По портальной системе инсулин достигает печени - своего главного органа-мишени. Печеночные рецепторы связывают половину секретированного гормона. Другая половина, попадая в системный кровоток, достигает мышц и жировой ткани. Большая часть инсулина (80 %) подвергается протеолитическому распаду в печени, остальная - в почках, и лишь незначительное количество метаболизируется непосредственно мышечными и жировыми клетками. В норме ПЖЖ
 Рис. 7.3.
Двухфазное высвобождение инсулина под воздействием глюкозы
Рис. 7.3.
Двухфазное высвобождение инсулина под воздействием глюкозы
взрослого человека секретирует 35-50 Ед инсулина в сутки, что составляет 0,6-1,2 Ед на 1 кг массы тела. Эта секреция подразделяется на пищевую и базальную. Пищевая секреция инсулина со ответствует постпрандиальному подъему уровня глюкозы, т.е. за счет нее обеспечивается нейтрализация гипергликемизирующего действия пищи. Количество пищевого инсулина примерно соответствует количеству принятых углеводов - около 1-2,5 Ед
на 10-12 г углеводов (1 хлебная единица - ХЕ). Базальная секреция инсулина обеспечивает оптимальный уровень гликемии и анаболизма в интервалах между едой и во время сна. Базальный инсулин секретируется со скоростью примерно 1 Ед/ч, при длительной физической нагрузке или длительном голодании она существенно уменьшается. На пищевой инсулин приходится не менее 50-70 % суточной продукции инсулина (рис. 7.4).
Секреция инсулина подвержена не только пищевым, но и суточ-
 Рис. 7.4.
Схема суточной продукции инсулина в норме
Рис. 7.4.
Схема суточной продукции инсулина в норме
ным колебаниям: потребность в инсулине повышается в ранние утренние часы, а в дальнейшем постепенно падает в течение дня. Так, на завтрак на 1 ХЕ секретируется 2,0-2,5 Ед инсулина, на обед - 1,0-1,5 Ед, а на ужин - 1,0 ЕД. Одной из причин такого изменения чувствительности к инсулину является высокий уровень ряда контринсулярных гормонов (в первую очередь кортизола) в утренние часы, который постепенно падает до минимального в начале ночи.
Основными физиологическими эффектами инсулина являются стимуляция переноса глюкозы через мембраны клеток инсулинзависимых тканей. Основными органами-мишенями инсулина являются печень, жировая ткань и мышцы. К инсулиннезависимым тканям, поступление глюкозы в которые не зависит от эффектов инсулина, в первую очередь относятся центральная и периферическая нервная система, эндотелий сосудов, клетки крови и др. Инсулин стимулирует синтез гликогена в печени и мышцах, синтез жиров в печени и жировой ткани, синтез белков в печени, мышцах и других органах. Все эти изменения направлены на утилизацию глюкозы, что приводит к снижению ее уровня в крови. Физиологическим антагонистом инсулина является глюкагон, который стимулирует мобилизацию гликогена и жиров из депо; в норме уровень глюкагона меняется реципрокно продукции инсулина.
Биологические эффекты инсулина опосредованы его рецепторами, которые расположены на клетках-мишенях. Рецептор инсулина представляет собой гликопротеин, состоящий из четырех субъединиц. При высоком уровне инсулина в крови число его рецепторов по принципу понижающей регуляции снижается, что сопровождается снижением чувствительности клетки к инсулину. После связывания инсулина с клеточным рецептором образовавшийся комплекс поступает внутрь клетки. Далее внутри мышечной и жировой клетки инсулин вызывает мобилизацию внутриклеточных везикул, которые содержат транспортер глюкозы GLUT-4. В результате этого везикулы перемещаются к клеточной поверхности, где GLUT-4 выполняет функцию входного отверстия для глюкозы. Аналогичное действие на GLUT-4 оказывает физическая нагрузка.
7.3. ЛАБОРАТОРНАЯ ДИАГНОСТИКА И КРИТЕРИИ КОМПЕНСАЦИИ САХАРНОГО ДИАБЕТА
Лабораторная диагностика СД базируется на определении уровня глюкозы крови, при этом критерии диагностики едины для всех
типов и вариантов СД (табл. 7.2). Данные других лабораторных исследований (уровень глюкозурии, определение уровня гликированного гемоглобина) для верификации диагноза СД использоваться не должны. Диагноз СД может быть установлен на основании двукратного обнаружения одного из трех критериев:
1. При явных симптомах СД (полиурия, полидипсия) и уровне глюкозы в цельной капиллярной крови более 11,1 ммоль/л вне зависимости от времени суток и предшествовавшего приема пищи.
2. При уровне глюкозы в цельной капиллярной крови натощак более 6,1 ммоль/л.
3. При уровне глюкозы в цельной капиллярной крови через 2 часа после приема 75 грамм глюкозы (оральный глюкозотолерантный тест) более 11,1 ммоль/л.
Табл. 7.2. Критерии диагностики сахарного диабета
 Наиболее
важным и значимым тестом в диагностике СД является определение уровня
гликемии натощак (минимум 8 часов голодания). В РФ уровень гликемии, как
правило, оценивается в цельной крови. Во многих странах широко
используется определение уровня глюкозы
Наиболее
важным и значимым тестом в диагностике СД является определение уровня
гликемии натощак (минимум 8 часов голодания). В РФ уровень гликемии, как
правило, оценивается в цельной крови. Во многих странах широко
используется определение уровня глюкозы
в плазме крови. Оральному глюкозотолерантному тесту (ОГТТ; определение уровня глюкозы через 2 часа после приема внутрь растворенных в воде 75 граммов глюкозы) в этом плане придается меньшее значение. Тем не менее на основании ОГТТ диагностируется нарушение толерантности к глюкозе (НТГ). НТГ диагностируется если уровень гликемии цельной капиллярной крови натощак не превышает 6,1 ммоль/л, а через 2 часа после нагрузки глюкозой оказывается выше 7,8 ммоль/ л, но ниже 11,1 ммоль/л. Другим вариантом нарушения углеводного обмена является нарушенная гликемия натощак (НГНТ). Последняя устанавливается если уровень гликемии цельной капиллярной крови натощак находится в пределах 5,6-6,0 ммоль/л, а через 2 часа после нагрузки глюкозой меньше 7,8 ммоль/л). НТГ и НГНТ в настоящее время объединяют термином предиабет, поскольку у обеих категорий пациентов высок риск манифестации СД и развития диабетической макроангиопатии.
Для диагностики СД уровень гликемии должен определяться стандартными лабораторными методами. При интерпретации показателей гликемии следует иметь в виду, что натощак уровень глюкозы в цельной венозной крови соответствует ее уровню в цельной капиллярной. После приема пищи или ОГТТ ее уровень в венозной крови примерно на 1,1 ммоль/л ниже, чем в капиллярной. Содержание глюкозы в плазме примерно на 0,84 ммоль/л выше, чем в цельной крови. С целью оценки компенсации и адекватности терапии СД уровень гликемии оценивается в капиллярной крови при помощи портативных глюкометров самими пациентами, их родственниками или медицинским персоналом.
При любом типе СД, а также при значительной нагрузке глюкозой может развиваться глюкозурия, которая является следствием превышения порога реабсорбции глюкозы из первичной мочи. Порог реабсорбции глюкозы значительно индивидуально варьирует (≈ 9-10 ммоль/л). Как отдельно взятый показатель глюкозурия для постановки диагноза СД использоваться не должна. В норме, за исключением случаев значительной пищевой нагрузки рафинированными углеводами, глюкозурия не встречается.
Продукция кетоновых тел (ацетон, ацетоацетат, β-гидроксибутират) значительно интенсифицируется при абсолютном дефиците инсулина. При декомпенсации СД-1 может определяться выраженная кетонурия (исследуется при помощи тест-полосок, которые опускаются в мочу). Легкая (следовая) кетонурия может определяться у здоровых людей при голодании и безуглеводной диете.
Важным лабораторным показателем, который используется для дифференциальной диагностики типов СД, а также для выявления формирования дефицита инсулина у пациентов с СД-2, является уровень С-пептида. По уровню С-пептида в крови можно косвенно судить об инсулинсекретирующей способности β-клеток ПЖЖ. Последние продуцируют проинсулин, от которого перед секрецией отщепляется С-пептид, попадающий в кровь в одинаковых количествах с инсулином. Инсулин на 50 % связывается в печени и имеет время полужизни в периферической крови около 4 мин. С-пептид из кровотока печенью не удаляется и имеет время полужизни в крови около 30 мин. Кроме того, он не связывается клеточными рецепторами на периферии. Поэтому определение уровня С-пептида является более надежным тестом для оценки функции инсулярного аппарата. Уровень С-пептида наиболее информативно исследовать на фоне стимуляционных проб (после приема пищи или введения глюкагона). Тест неинформативен, если он проводится на фоне выраженной декомпенсации СД, поскольку выраженная гипергликемия оказывает токсическое действие на β-клетки (глюкозотоксичность). Инсулинотерапия в течение нескольких предшествовавших дней на результаты теста никак не повлияет.
Основной целью лечения любого типа СД является предотвращение его поздних осложнений, которое может быть достигнуто на фоне его стабильной компенсацией по ряду параметров (табл. 7.3). Основным критерием качества компенсации углеводного обмена при СД является уровень гликированного (гликозилированного) гемоглобина (HbA1c). Последний представляет собой гемоглобин, нековалентно связанный с глюкозой. В эритроциты глюкоза поступает независимо от инсулина, и гликозилирование гемоглобина является необратимым процессом, а его степень прямо пропорциональна концентрации глюкозы, с которой он контактировал на протяжении 120 дней своего существования. Небольшая часть гемоглобина гликозилируется и в норме; при СД она может быть значительно повышена. Уровень HbA1c, в отличие от уровня глюкозы, который постоянно меняется, интегрально отражает гликемию на протяжении последних 3-4 месяцев. Именно с таким интервалом и рекомендуется определение уровня HbA1c с целью оценки компенсации СД.
Хроническая гипергликемия является далеко не единственным фактором риска развития и прогрессирования поздних осложнений СД. В связи с этим оценка компенсации СД базируется на комплексе
лабораторных и инструментальных методов исследования (табл. 7.3). Помимо показателей, характеризующих состояние углеводного обмена, наиболее важное значение имеют уровень артериального давления и липидный спектр крови.
Табл. 7.3. Критерии компенсации сахарного диабета
 Помимо
приведенных критериев компенсации, при планировании целей лечения СД
необходим индивидуальный подход. Вероятность развития и прогрессирования
поздних осложнений СД (особенно микроангиопатии) возрастает с
увеличением длительности заболевания. Таким образом, если у детей и
молодых пациентов, стаж диабета которых в дальнейшем может достигнуть
нескольких десятков лет, необходимо добиваться оптимальных показателей
гликемии, то у пациентов, у которых СД манифестировал в пожилом и
старческом возрасте, жесткая эугликемическая компенсация, значительно
повышающая риск гипогликемий, не всегда целесообразна.
Помимо
приведенных критериев компенсации, при планировании целей лечения СД
необходим индивидуальный подход. Вероятность развития и прогрессирования
поздних осложнений СД (особенно микроангиопатии) возрастает с
увеличением длительности заболевания. Таким образом, если у детей и
молодых пациентов, стаж диабета которых в дальнейшем может достигнуть
нескольких десятков лет, необходимо добиваться оптимальных показателей
гликемии, то у пациентов, у которых СД манифестировал в пожилом и
старческом возрасте, жесткая эугликемическая компенсация, значительно
повышающая риск гипогликемий, не всегда целесообразна.
7.4. ПРЕПАРАТЫ ИНСУЛИНА И ИНСУЛИНОТЕРАПИЯ
Препараты инсулина жизненно необходимы пациентам с СД-1; кроме того, их получает до 40 % пациентов с СД-2. К общим показаниям для назначения инсулинотерапии при СД, многие из которых фактически перекрываются одно другим, относятся:
1. Сахарный диабет 1 типа
2. Панкреатэктомия
3. Кетоацидотическая и гиперосмолярная кома
4. При сахарном диабете 2 типа:
Явные признаки дефицита инсулина, такие как прогрессирующееснижение массы тела и кетоз, выраженная гипергликемия;
Большие хирургические вмешательства;
Острые макроваскулярные осложнения (инсульт, инфаркт миокарда, гангрена и пр.) и тяжелые инфекционные заболевания, сопровождающиеся декомпенсацией углеводного обмена;
Уровень гликемии натощак более 15-18 ммоль/л;
Отсутствие стойкой компенсации, несмотря на назначение максимальных суточных доз различных таблетированных сахароснижающих препаратов;
Поздние стадии поздних осложнений СД (тяжелая полинейропатия и ретинопатия, хроническая почечная недостаточность).
5. Невозможность добиться компенсации гестационного СД с помощью диетотерапии.
По происхождению препараты инсулина могут быть классифицированы на три группы:
Животные инсулины (свиные);
Человеческие инсулины (полусинтетические, генно-инженерные);
Аналоги инсулинов (лизпро, аспарт, гларгин, детемир).
Прогресс технологий производства человеческих инсулинов привел к тому, что использование свиных инсулинов (отличается от человеческого одной аминокислотой) в последнее время существенно сократилось. Свиной инсулин может быть использован для производства человеческого инсулина полусинтетическим методом, который подразумевает замену одной отличающейся аминокислоты в его молекуле. Наиболее высоким качеством отличаются генно-инженерные человеческие инсулины. Для их получения участок генома человека, ответственный за синтез инсулина, ассоциируют с геномом E.coli или дрожжевой культуры, в результате чего последние начинают продуцировать человеческий инсулин. Создание аналогов инсулина при помощи перестановок различных аминокислот преследовало цель получения препаратов с заданной и наиболее благоприятной фармакокинетикой. Так, инсулин лизпро (Хумалог) является аналогом
инсулина ультракороткого действия, при этом его сахароснижающий эффект развивается уже спустя 15 минут после инъекции. Аналог инсулина гларгин (Лантус), напротив, характеризуется длительным действием, которое продолжается на протяжении суток, при этом особенностью кинетики препарата является отсутствие выраженных пиков концентрации в плазме. Большинство использующихся в настоящее время препаратов инсулина и его аналогов выпускаются в концентрации 100 Ед/мл. По длительности действия инсулины подразделяются на 4 основные группы (табл. 7.4):
Табл. 7.4. Фармакокинетика препаратов и аналогов инсулина
 1.
Ультракороткого действия (лизпро, аспарт).
1.
Ультракороткого действия (лизпро, аспарт).
2. Короткого действия (простой человеческий инсулин).
3. Средней продолжительности действия (инсулины на нейтральном протамине Хагедорна).
4. Длительного действия (гларгин, детемир).
5. Смеси инсулинов различной продолжительности действия (Новомикс-30, Хумулин-МЗ, Хумалог-Микс-25).
Препараты ультракороткого действия [лизпро (Хумалог), аспарт (Новорапид)] являются аналогами инсулина. Их преимуществами являются быстрое развитие сахароснижающего эффекта после инъекции (через 15 минут), что позволяет делать инъекцию непосредственно перед едой или даже сразу после еды, а также короткая продолжительность действия (менее 3 часов), что снижает риск развития гипогликемии. Препараты короткого действия (простой инсулин, инсулин-регуляр) представляют собой раствор, содержащий инсулин в концентрации 100 Ед/мл. Инъекция простого инсулина делается за 30 минут до еды; длительность действия составляет порядка 4-6 часов. Препараты ультракороткого и короткого действия могут вводиться подкожно, внутримышечно и внутривенно.
Среди препаратов средней продолжительности действия чаще всего используются препараты на нейтральном протамине Хагедорна (НПХ). НПХ представляет собой белок, который нековалентно адсорбирует инсулин, замедляя его всасывание из подкожного депо. Эффективная продолжительность действия инсулинов НПХ обычно составляет около 12 часов; они вводятся только подкожно. Инсулин НПХ представляет собой суспензию, в связи с чем в отличие от простого инсулина во флаконе он мутный, а при длительной стоянии образуется взвесь, которую необходимо тщательно перемешать перед инъекцией. Инсулины НПХ в отличие от других препаратов пролонгированного действия можно в любых соотношениях смешивать с инсулином короткого действия (простым инсулином), при этом фармакокинетика компонентов смеси не изменится, поскольку НПХ не будет связывать дополнительные количества простого инсулина (рис. 7.5). Кроме того, протамин используется для приготовления стандартных смесей аналогов инсулина (Новомикс-30, Хумалог-Микс-25).
Среди препаратов длительного действия в настоящее время активно используют аналоги инсулина гларгин (Лантус) и детемир (Левемир). Благоприятная особенность фармакокинетики этих препаратов заключается в том, что в отличие от инсулинов НПХ они обеспечивают более равномерное и длительное поступление препарата из подкожного депо. В связи с этим гларгин может назначаться всего один раз в день, при этом практически независимо от времени суток.
 Рис. 7.5.
Фармакококинетика различных препаратов инсулина:
Рис. 7.5.
Фармакококинетика различных препаратов инсулина:
а) монокомпонентных; б) стандартных смесей инсулинов
Помимо монокомпонентных препаратов инсулина, в клинической практике широко используются стандартные смеси. Как правило, речь идет о смесях короткого или ультракороткого инсулина с инсулином средней продолжительности действия. Например, препарат «Хумулин-МЗ» содержит в одном флаконе 30 % простого инсулина и 70 % инсулина НПХ; препарат «Новомикс-30» содержит 30 % инсулина аспарт и 70 % кристаллической протаминовой суспензии инсулина аспарт; препарат «Хумалог-Микс-25» содержит 25 % инсулина лизпро и 75 % протаминовой суспензии инсулина лизпро. Преимуществом
стандартных смесей инсулинов является замена двух инъекций одной и несколько большая точность дозировки компонентов смеси; недостатком - невозможность индивидуального дозирования отдельных компонентов смеси. Это определяет предпочтительность использования стандартных смесей инсулинов для терапии СД-2 или при так называемой традиционной инсулинотерапии (назначение фиксированных доз инсулинов), тогда как для интенсивной инсулинотерапии (гибкий подбор дозы в зависимости от показателей гликемии и количества углеводов в пище) предпочтительнее использование монокомпонентных препаратов.
Залогом успешной инсулинотерапии является четкое соблюдение техники инъекций. Существует несколько способов введения инсулина. Наиболее простой и при этом надежный метод - инъекции при помощи инсулинового шприца. Более удобным способом введения инсулина являются инъекции при помощи шприц-ручки, которая представляет собой комбинированное устройство, содержащее резервуар с инсулином (картридж), систему дозирования и иглу с инжектором.
Для поддерживающей терапии (когда речь не идет о выраженной декомпенсации СД или о критических состояниях) инсулин вводится подкожно. Инъекции инсулина короткого действия рекомендуется делать в подкожную жировую клетчатку живота, инсулина пролонгированного действия - в клетчатку бедра или плеча (рис. 7.6 а). Инъекции делаются глубоко в подкожную клетчатку через широко сжатую кожу под углом в 45° (рис. 7.6 б). Пациенту необходимо рекомендовать ежедневную смену мест введения инсулина в пределах одной области в целях предупреждения развития липодистрофий.
К факторам, влияющим на скорость абсорбции инсулина из подкожного депо, следует отнести дозу инсулина (увеличение дозы увеличивает продолжительность абсорбции), место инъекции (абсорбция быстрее из клетчатки живота), температура окружающей среды (согревание и массаж места инъекции ускоряет абсорбцию).
Более сложным методом введения, который, тем не менее, у многих пациентов позволяет достигнуть хороших результатов лечения, является использование дозатора инсулина, или системы для непрерывного подкожного введения инсулина. Дозатор представляет собой портативный прибор, состоящий из компьютера, который задает режим подачи инсулина, а также системы подачи инсулина, осуществляющейся по катетеру и миниатюрной игле в подкожную
 Рис. 7.6.
Инъекции инсулина: а) типичные места инъекций; б) положение иглы инсулинового шприца при инъекции
Рис. 7.6.
Инъекции инсулина: а) типичные места инъекций; б) положение иглы инсулинового шприца при инъекции
жировую клетчатку. При помощи дозатора осуществляется непрерывное базальное введение инсулина короткого или ультракороткого действия (скорость порядка 0,5-1 Ед/час), а перед приемом пищи в зависимости от содержания в ней углеводов и уровня гликемии пациент вводит необходимую болюсную дозу того же инсулина короткого действия. Преимуществом инсулинотерапии с помощью дозатора является введение одного только инсулина короткого (или даже ультракороткого) действия, что само по себе несколько более физиологично, поскольку абсорбция пролонгированных препаратов инсулина подвергается большим колебаниям; в связи с этим непрерывное введение инсулина короткого действия оказывается более управляемым процессом. Недостатком инсулинотерапии при помощи дозатора является необходимость постоянного ношения прибора, а также длительное нахождение инъекционной иглы в подкожной клетчатке, требующее периодического контроля за процессом подачи инсулина. Инсулинотерапия при помощи дозатора в первую очередь показана пациентам с СД-1, которые готовы овладеть техникой ее ведения. Особенно в этом плане следует обращать внимание на пациентов с выраженным феноменом «утренней зари», а также на беременных и планирующих беременность пациенток с СД-1 и паци-
ентов с неупорядоченным образом жизни (возможность более гибкого режима питания).
7.5. САХАРНЫЙ ДИАБЕТ 1 ТИПА
СД-1 - органоспецифическое аутоиммунное заболевание, приводящее к деструкции инсулинпродуцирующих β-клеток островков ПЖЖ, проявляющееся абсолютным дефицитом инсулина. В ряде случаев у пациентов с явным СД-1 отсутствуют маркеры аутоиммунного поражения β-клеток (идиопатический СД-1).
Этиология
СД-1 является заболеванием с наследственной предрасположенностью, но ее вклад в развитие заболевания невелик (определяет его развитие примерно на 1 /з). Конкордантность у однояйцевых близнецов по СД-1 составляет всего 36 %. Вероятность развития СД-1 у ребенка при больной матери составляет 1-2 %, отце - 3-6 %, брате или сестре - 6 %. Одни или несколько гуморальных маркеров аутоиммунного поражения β-клеток, к которым относятся антитела к островкам ПЖЖ, антитела к глутамат-декарбоксилазе (GAD65) и антитела к тирозин-фосфатазе (IA-2 и ΙΑ-2β), обнаруживаются у 85-90 % пациентов. Тем не менее основное значение в деструкции β-клеток придается факторам клеточного иммунитета. СД-1 ассоциирован с такими гаплотипами HLA, как DQA и DQB, при этом одни аллели HLA-DR/DQ могут быть предрасполагающими к развитию заболевания, тогда как другие - протективными. С повышенной частотой СД-1 сочетается с другими аутоиммунными эндокринными (аутоиммунный тиреоидит, болезнь Аддисона) и неэндокринными заболеваниями, такими как алопеция, витилиго, болезнь Крона, ревматические заболевания (табл. 7.5).
Патогенез
СД-1 манифестирует при разрушении аутоиммунным процессом 80-90 % β-клеток. Скорость и интенсивность этого процесса может существенно варьировать. Наиболее часто при типичном течении заболевания у детей и молодых людей этот процесс протекает достаточно быстро с последующей бурной манифестацией заболевания, при которой от появления первых клинических симптомов до развития кетоацидоза (вплоть до кетоацидотической комы) может пройти всего несколько недель.
Табл. 7.5. Сахарный диабет 1 типа
 Продолжение табл. 7.5
Продолжение табл. 7.5
 В других, значительно более редких случаях, как правило, у взрослых старше 40 лет, заболевание может протекать латентно (латентный аутоиммунный диабет взрослых - LADA),
при
этом в дебюте заболевания таким пациентам нередко устанавливается
диагноз СД-2, и на протяжении нескольких лет компенсация СД может
достигаться назначением препаратов сульфонилмочевины. Но в дальнейшем,
обычно спустя 3 года, появляются признаки абсолютного дефицита инсулина
(похудение, кетонурия, выраженная гипергликемия, несмотря на прием
таблетированных сахароснижающих препаратов).
В других, значительно более редких случаях, как правило, у взрослых старше 40 лет, заболевание может протекать латентно (латентный аутоиммунный диабет взрослых - LADA),
при
этом в дебюте заболевания таким пациентам нередко устанавливается
диагноз СД-2, и на протяжении нескольких лет компенсация СД может
достигаться назначением препаратов сульфонилмочевины. Но в дальнейшем,
обычно спустя 3 года, появляются признаки абсолютного дефицита инсулина
(похудение, кетонурия, выраженная гипергликемия, несмотря на прием
таблетированных сахароснижающих препаратов).
В основе патогенеза СД-1, как указывалось, лежит абсолютный дефицит инсулина. Невозможность поступления глюкозы в инсулинзависимые ткани (жировая и мышечная) приводит к энергетической недостаточности в результате чего интенсифицируется липолиз и протеолиз, с которыми связана потеря массы тела. Повышение уровня гликемии вызывает гиперосмолярность, что сопровождается осмотическим диурезом и выраженным обезвоживанием. В условиях дефицита инсулина и энергетической недостаточности растормаживается продукция контринсулярных гормонов (глюкагон, кортизол, гормон роста), которая, несмотря на нарастающую гликемию, обусловливает стимуляцию глюконеогенеза. Усиление липолиза в жировой ткани приводит к значительному увеличению концентрации свободных жирных кислот. При дефиците инсулина липосинтетическая способность печени оказывается подавленной, и свобод-
ные жирные кислоты начинают включаться в кетогенез. Накопление кетоновых тел приводит к развитию диабетического кетоза, а в дальнейшем - кетоацидоза. При прогрессирующем нарастании обезвоживания и ацидоза развивается коматозное состояние (см. п. 7.7.1), которое при отсутствии инсулинотерапии и регидратации неизбежно заканчивается смертью.
Эпидемиология
На СД-1 приходится порядка 1,5-2 % всех случаев диабета, и этот относительный показатель в дальнейшем будет уменьшаться в силу быстрого роста заболеваемости СД-2. Риск развития СД-1 на протяжении жизни у представителя белой расы составляет около 0,4 %. Заболеваемость СД-1 увеличивается на 3 % в год: на 1,5 % - за счет новых случаев и еще на 1,5 % - за счет увеличения продолжительности жизни пациентов. Распространенность СД-1 варьирует в зависимости от этнического состава популяции. На 2000 год она составила 0,02 % в Африке, 0,1 % в Южной Азии, а также в Южной и Центральной Америке и 0,2 % в Европе и Северной Америке. Наиболее высока заболеваемость СД-1 в Финляндии и Швеции (30-35 случаев на 100 тысяч населения в год), а наиболее низка в Японии, Китае и Корее (соответственно 0,5-2,0 случая). Возрастной пик манифестации СД-1 соответствует примерно 10-13 годам. В подавляющем большинстве случаев СД-1 манифестирует до 40 лет.
Клинические проявления
В типичных случаях, особенно у детей и молодых людей, СД-1 дебютирует яркой клинической картиной, которая развивается на протяжении нескольких месяцев или даже недель. Манифестацию СД-1 могут спровоцировать инфекционные и другие сопутствующие заболевания. Характерны общие для всех типов СД симптомы, связанные с гипергликемией: полидипсия, полиурия, кожный зуд, но при СД-1 они очень ярко выражены. Так, на протяжении дня пациенты могут выпивать и выделять до 5-10 литров жидкости. Специфичным для СД-1 симптомом, который обусловлен абсолютным дефицитом инсулина, является похудение, достигающее 10-15 кг на протяжении 1-2 месяцев. Характерна выраженная общая и мышечная слабость, снижение работоспособности, сонливость. В начале заболевания у некоторых пациентов может отмечаться повышение аппетита, которое сменяется анорексией по мере развития кетоацидоза. Последний характеризуется появлением запаха ацетона (или фруктового запаха) изо рта, тош-
нотой, рвотой, нередко болями в животе (псевдоперитонит), тяжелым обезвоживанием и заканчивается развитием коматозного состояния (см. п. 7.7.1). В ряде случаев первым проявлением СД-1 у детей является прогрессирующее нарушение сознания вплоть до комы на фоне сопутствующих заболеваний, как правило, инфекционных или острой хирургической патологии.
В относительно редких случаях развития СД-1 у лиц старше 35-40 лет (латентный аутоиммунный диабет взрослых) заболевание может манифестировать не столь ярко (умеренная полидипсия и полиурия, отсутствие потери массы тела) и даже выявляться случайно при рутинном определении уровня гликемии. В этих случаях пациенту нередко в начале устанавливается диагноз СД-2 и назначаются таблетированные сахароснижающие препараты (ТСП), которые какое-то время обеспечивают приемлемую компенсацию СД. Тем не менее на протяжении нескольких лет (часто в течение года) у пациента появляются симптомы, обусловленные нарастающим абсолютным дефицитом инсулина: похудение, невозможность поддержания нормальной гликемии на фоне ТСП, кетоз, кетоацидоз.
Диагностика
Учитывая, что СД-1 имеет яркую клиническую картину, а также является относительно редким заболеванием, скрининговое определение уровня гликемии с целью диагностики СД-1 не показано. Вероятность развития заболевания у ближайших родственников пациентов невысока, что вместе с отсутствием эффективных методов первичной профилактики СД-1 определяет нецелесообразность изучения у них иммуногенетических маркеров заболевания. Диагностика СД-1 в подавляющем большинстве случаев базируется на выявлении значительной гипергликемии у пациентов с выраженными клиническими проявлениями абсолютного дефицита инсулина. ОГТТ с целью диагностики СД-1 приходится проводить очень редко.
Дифференциальная диагностика
В сомнительных случаях (выявление умеренной гипергликемии при отсутствии явных клинических проявлений, манифестация в относительно немолодом возрасте), а также с целью дифференциальной диагностики с другими типами СД используется определение уровня С-пептида (базального и через 2 часа после приема пищи). Косвенное диагностическое значение в сомнительных случаях может иметь определение иммунологических маркеров СД-1 - антитела к островкам
ПЖЖ, к глутаматдекарбоксилазе (GAD65) и тирозинфосфатазе (IA-2 и IA-2β). Дифференциальная диагностика СД-1 и СД-2 представлена в табл. 7.6.
Табл. 7.6. Дифференциальная диагностика и отличия СД-1 и СД-2
 Лечение
Лечение
Лечение любого типа СД базируется на трех основных принципах: сахароснижающая терапия (при СД-1 - инсулинотерапия), диета и обучение пациентов. Инсулинотерапия при СД-1 носит заместительный характер и ее целью является максимальная имитация физиологической продукции гормона с целью достижения принятых критериев компенсации (табл. 7.3). К физиологической секреции инсулина наиболее приближена интенсивная инсулинотерапия. Потребность в инсулине, соответствующая его базальной секреции, обеспечивается двумя инъекциями инсулина средней продолжительности действия (утром и вечером) или одной инъекцией инсулина длительного действия (гларгин). Суммарная доза базального инсу-
лина не должна превышать половины всей суточной потребности в препарате. Пищевая или болюсная секреция инсулина замещается инъекциями инсулина короткого или ультракороткого действия перед каждым приемом пищи, при этом его доза рассчитывается, исходя из количества углеводов, которое предполагается принять во время предстоящего приема пищи, и имеющегося уровня гликемии, определяемого пациентом с помощью глюкометра перед каждой инъекцией инсулина (рис. 7.7).
Ориентировочная схема интенсивной инсулинотерапии, которая будет меняться практически каждый день, может быть представлена следующим образом. Исходят из того, что суточная потребность в инсулине составляет около 0,5-0,7 Ед на 1 кг массы тела (для пациента с массой тела 70 кг около 35-50 Ед). Около 1 /з - 1 /2 этой дозы составит инсулин пролонгированного действия (20-25 Ед), 1 /2 - 2 /з инсулин короткого или ультракороткого действия. Доза инсулина НПХ делится на 2 инъекции: утром 2 /з его дозы (12 Ед), вечером - 1 /з (8-10 Ед).
Целью первого этапа подбора инсулинотерапии является нормализация уровня глюкозы натощак. Вечерняя доза инсулина НПХ обычно вводится в 22-23 часа, утренняя вместе с инъекцией инсулина короткого действия перед завтраком. При подборе вечерней дозы инсулина НПХ необходимо иметь в виду возможность развития ряда
 Рис. 7.7.
Схема интенсивной инсулинотерапии
Рис. 7.7.
Схема интенсивной инсулинотерапии
достаточно типичных феноменов. Причиной утренней гипергликемии может быть недостаточнсть дозы инсулина пролонгированного действия, поскольку к утру потребность в инсулине существенно возрастает (феномен «утренней зари»). Помимо недостаточности дозы к утренней гипергликемии может привести ее избыток - феномен Сомоджи (Somogyi), постгипогликемическая гипергликемия. Этот феномен объясняется тем, что максимальная чувствительность тканей к инсулину отмечается между 2 и 4 часами ночи. Именно в это время уровень основных контринсулярных гормонов (кортизол, гормон роста и др.) в норме наиболее низок. Если вечерняя доза инсулина пролонгированного действия избыточна, то в это время развивается гипогликемия. Клинически она может проявляться плохим сном с кошмарными сновидениями, бессознательными действиями во сне, утренней головной болью и разбитостью. Развитие в это время гипогликемии вызывает значительный компенсаторный выброс глюкагона и других контринсулярных гормонов с последующей гипергликемией в утренние часы. Если в этой ситуации не снизить, а увеличить дозу пролонгированного инсулина, вводимого вечером, ночная гипогликемия и утренняя гипергликемия будут усугубляться, что в итоге может привести к синдрому хронической передозировки инсулина (синдром Сомоджи), который представляет собой сочетание ожирения с хронической декомпенсацией СД, частыми гипогликемиями и прогрессирующими поздними осложнениями. Для диагностики феномена Сомоджи необходимо исследование уровня гликемии около 3 ч ночи, которое является неотъемлемым компонентом подбора инсулинотерапии. Если снижение вечерней дозы НПХ до безопасной в плане развития ночной гипогликемии сопровождается гипергликемией утром (феномен утренней зари), пациенту необходимо рекомендовать более ранний подъем (6-7 утра), в то время, когда введенный на ночь инсулин еще продолжает поддерживать нормальный уровень гликемии.
Вторая инъекция инсулина НПХ обычно делается перед завтраком вместе с утренней инъекцией инсулина короткого (ультракороткого) действия. В данном случае доза подбирается преимущественно исходя из показателей уровня гликемии перед основными дневными приемами пищи (обед, ужин); кроме того, ее может лимитировать развитие гипогликемий в промежутках между приемами пищи, например в полдень, между завтраком и обедом.
Вся доза инсулина пролонгированного действия (гларгин) вводится одни раз в день, при этом не принципиально, в какое время. Кинетика
инсулинов гларгин и детемир более благоприятна в плане риска развития гипогликемий, в том числе ночных.
Доза инсулина короткого или ультракороткого действия даже в первый для пациента день назначения инсулина будет зависеть от количества употребляемых углеводов (хлебных единиц) и уровня гликемии перед инъекцией. Условно, исходя из суточного ритма секреции инсулина в норме, около 1 / 4 дозы инсулина короткого действия (6-8 ЕД) отводится на ужин, оставшаяся доза примерно поровну разделится на завтрак и обед (10-12 ЕД). Чем выше исходный уровень гликемии, тем меньше он будет снижаться на единицу вводимого инсулина. Инъекция инсулина короткого действия делается за 30 минут до еды, ультракороткого действия непосредственно перед едой или даже сразу после еды. Адекватность дозы инсулина короткого действия оценивается по показателям гликемии через 2 часа после еды и перед очередным приемом пищи.
Для расчета дозы инсулина при интенсивной инсулинотерапии достаточно подсчета числа ХЕ, исходя только из углеводного компонента. При этом в расчет берутся не все углеводсодержащие продукты, а только так называемые подсчитываемые. К последним относятся картофель, зерновые продукты, фрукты, жидкие молочные и сладкие продукты. Продукты, содержащие неусваиваемые углеводы (большинство овощей), в расчет не берутся. Разработаны специальные обменные таблицы, с помощью которых, выражая количество углеводов в ХЕ, можно рассчитать необходимую дозу инсулина. Одной ХЕ соответствует 10-12 г углеводов (табл. 10.7).
После приема пищи, содержащей 1 ХЕ, уровень гликемии увеличивается на 1,6-2,2 ммоль/л, т.е. примерно на столько, на сколько снижается уровень глюкозы при введении 1 Ед инсулина. Другими словами, на каждую ХЕ, содержащуюся в пище, которую планируется съесть, необходимо заранее ввести (в зависимости от времени суток) около 1 Ед инсулина. Кроме того, необходим учет результатов самоконтроля уровня гликемии, который производится перед каждой инъекцией, и времени суток (около 2 Ед инсулина на 1 ХЕ утром и в обед, 1 Ед на 1 ХЕ - на ужин). Так, если выявлена гипергликемия, дозу инсулина, рассчитанную в соответствии с предстоящим приемом пищи (по числу ХЕ), нужно увеличить, и наоборот, если выявлена гипогликемия, инсулина вводится меньше.
Табл. 7.7. Эквивалентная замена продуктов, составляющих 1 ХЕ
 Например,
если у пациента за 30 мин до планируемого ужина, содержащего 5 ХЕ,
уровень гликемии составляет 7 ммоль/л, ему необходимо ввести 1 Ед
инсулина для того, чтобы гликемия снизилась до нормального уровня: с 7
ммоль/л примерно до 5 ммоль/л. Кроме того, 5 Ед инсулина необходимо
ввести на покрытие 5 ХЕ. Таким образом, пациент в данном случае введет 6
Ед инсулина короткого или ультракороткого действия.
Например,
если у пациента за 30 мин до планируемого ужина, содержащего 5 ХЕ,
уровень гликемии составляет 7 ммоль/л, ему необходимо ввести 1 Ед
инсулина для того, чтобы гликемия снизилась до нормального уровня: с 7
ммоль/л примерно до 5 ммоль/л. Кроме того, 5 Ед инсулина необходимо
ввести на покрытие 5 ХЕ. Таким образом, пациент в данном случае введет 6
Ед инсулина короткого или ультракороткого действия.
После манифестации СД-1 и начала инсулинотерапии на протяжении достаточно длительного времени потребность в инсулине может быть небольшой и составлять менее 0,3-0,4 Ед/кг. Этот период обозначается как фаза ремиссии, или «медовый месяц». После периода гипергликемии и кетоацидоза, которые подавляют секрецию инсулина 10-15 % сохранившимися β-клетками, компенсация гормональнометаболических нарушений введением инсулина восстанавливает функцию этих клеток, которые затем берут на себя обеспечение организма инсулином на минимальном уровне. Этот период может продолжаться от нескольких недель до нескольких лет, но в конечном счете, вследствие аутоиммунной деструкции оставшихся β-клеток, «медовый месяц» заканчивается.
Диета при СД-1 у обученных пациентов, которые владеют навыками самоконтроля и подбора дозы инсулина, может быть либерализованной, т.е. приближающейся к свободной. Если у пациента отсутствует избыток или дефицит массы тела, диета должна быть
изокалорийной. Основным компонентом пищи при СД-1 являются углеводы, на которые должно приходиться около 65 % суточного калоража. Предпочтение следует отдавать продуктам, содержащим сложные, медленно всасывающиеся углеводы, а также продуктам, богатым пищевой клетчаткой. Продукты, содержащие легкоусваемые углеводы (мучное, сладкое), следует избегать. Доля белков должна быть снижена до 10-35 %, что способствует снижению риска развития микроангиопатии, а доля жиров - до 25-35 %, при этом на предельные жиры должно приходиться до 7 % калоража, что снижает риск развития атеросклероза. Кроме того, необходимо избегать приема алкогольных напитков, особенно крепких.
Неотъемлемым компонентом работы с пациентом с СД-1 и залогом его эффективной компенсации является обучение пациентов. На протяжении всей жизни пациент ежедневно должен самостоятельно в зависимости от многочисленных факторов изменять дозу инсулина. Очевидно, что это требует владения определенными навыками, которым пациента необходимо обучить. «Школа пациента с СД-1» организуется в эндокринологических стационарах или амбулаторно и представляет собой 5-7 структурированных занятий, на которых врач или специально обученная медсестра в интерактивном режиме с использованием различных наглядных пособий проводит обучение пациентов принципам самоконтроля.
Прогноз
При отсутствии инсулинотерапии больной СД-1 неизбежно погибает от кетоацидотической комы. При неадекватной инсулинотерапии, на фоне которой не достигаются критерии компенсации СД и пациент находится в состоянии хронической гипергликемии (табл. 7.3), начинают развиваться и прогрессировать поздние осложнения (п. 7.8). При СД-1 наибольшее клиническое значение в этом плане имеют проявления диабетической микроангиопатии (нефропатия и ретинопатия) и нейропатии (синдром диабетической стопы). Макроангиопатия при СД-1 на первый план выходит относительно редко.
7.6. САХАРНЫЙ ДИАБЕТ 2 ТИПА
Сахарный диабет 2 типа - хроническое заболевание, проявляющееся нарушением углеводного обмена с развитием гипергликемии вследствие инсулинорезистентности и секреторной дисфункции β-клеток,
а также липидного обмена с развитием атеросклероза. Поскольку основной причиной смерти и инвалидизации пациентов являются осложнения системного атеросклероза, СД-2 иногда называют сердечно-сосудистым заболеванием.
Табл. 7.8. Сахарный диабет 2 типа
 Этиология
Этиология
СД-2 является многофакторным заболеванием с наследственной предрасположенностью. Конкордатность по СД-2 у однояйцевых близнецов достигает 80 % и более. Большинство пациентов с СД-2 указывают на наличие СД-2 у ближайших родственников; при наличии СД-2 у одного из родителей вероятность его развития у потомка на протяжении жизни составляет 40 %. Какого-то одного гена, полиморфизм которого определяет предрасположенность к СД-2, не обнаружено. Большое значение в реализации наследственной предрасположенности к СД-2 играют факторы окружающей среды, в первую очередь, особенности образа жизни. Факторами риска развития СД-2 являются:
Ожирение, особенно висцеральное (см. п. 11.2);
Этническая принадлежность (особенно при смене традиционного образа жизни на западный);
Малоподвижный образ жизни;
Особенности диеты (высокое потребление рафинированных углеводов и низкое содержание клетчатки);
Артериальная гипертензия.
Патогенез
Патогенетически СД-2 представляет собой гетерогенную группу нарушений обмена веществ, именно это и определяет его значительную клиническую неоднородность. В основе его патогенеза лежит инсулинорезистентность (снижение опосредованной инсулином утилизации глюкозы тканями), которая реализуется на фоне секреторной дисфункции β-клеток. Таким образом, происходит нарушение баланса чувствительности к инсулину и инсулиновой секреции. Секреторная дисфункция β-клеток заключается в замедлении «раннего» секреторного выброса инсулина в ответ на увеличение уровня глюкозы в крови. При этом 1-я (быстрая) фаза секреции, которая заключается в опорожнении везикул с накопленным инсулином, фактически отсутствует; 2-я (медленная) фаза секреции осуществляется в ответ на стабилизирующуюся гипергликемию постоянно, в тоническом режиме, и, несмотря на избыточную секрецию инсулина, уровень гликемии на фоне инсулинорезистентности не нормализуется (рис. 7.8).
Следствием гиперинсулинемии является снижение чувствительности и числа инсулиновых рецепторов, а также подавление
пострецепторных механизмов, опосредующих эффекты инсулина (инсулинорезистентность). Содержание основного транспортера глюкозы в мышечных и жировых клетках (GLUT-4) снижено на 40 % у лиц с висцеральных ожирением и на 80 % - у лиц с СД-2. Вследствие инсулинорезистентности гепатоцитов и портальной гиперинсулинемией происходит гиперпродукция глюкозы печенью, и развивается гипергликемия натощак, которая выявляется у большинства пациентов с СД-2, в том числе и на ранних этапах заболевания.
Сама по себе гипергликемия неблагоприятно влияет на характер и уровень секреторной активности β-клеток (глюкозотоксичность). Длительно, на протяжении многих лет и десятилетий существующая гипергликемия в конечном счете приводит к истощению продукции инсулина β-клетками и у пациента могут появиться некоторые симптомы дефицита инсулина - похудение, кетоз при сопутствующих инфекционных заболеваниях. Тем не менее, остаточная продукция инсулина, которой оказывается достаточно для предотвращения кетоацидоза, при СД-2 практически всегда сохраняется.
Эпидемиология
СД-2 определяет эпидемиологию СД в целом, поскольку на него приходится около 98 % случаев этого заболевания. Распространенность СД-2 варьирует в разных странах и этнических группах. В европейских
 Рис. 7.8.
Секреторная дисфункция β-клеток при сахарном диабете 2 типа (выпадение 1-й быстрой фазы секреции инсулина)
Рис. 7.8.
Секреторная дисфункция β-клеток при сахарном диабете 2 типа (выпадение 1-й быстрой фазы секреции инсулина)
странах, США и Российской Федерации она составляет около 5-6 % населения. С возрастом заболеваемость СД-2 увеличивается: среди взрослых распространенность СД-2 составляет 10 %, среди лиц старше 65 лет достигает 20 %. Заболеваемость СД-2 в 2,5 раза выше среди коренных жителей Америки и Гавайских островов; среди индейцев племени Пима (штат Аризона) она достигает 50 %. Среди сельского населения Индии, Китая, Чили и Африканских стран, которые ведут традиционный образ жизни, распространенность СД-2 очень низка (менее 1 %). С другой стороны, среди переселенцев в западные индустриальные страны она достигает значительного уровня. Так, среди выходцев из Индии и Китая, проживающих в США и Великобритании, распространенность СД-2 достигает 12-15 %.
ВОЗ предсказывает увеличение числа больных диабетом в мире на 122 % в течение ближайших 20 лет (с 135 до 300 миллионов). Это связано как с прогрессирующим старением населения, так и с распространением и усугублением урбанизированного образа жизни. В последние годы отмечается значительное «омоложение» СД-2 и рост его заболеваемости среди детей.
Клинические проявления
В большинстве случаев, выраженные клинические проявления отсутствуют, и диагноз устанавливается при рутинном определении уровня гликемии. Заболевание обычно манифестирует в возрасте старше 40 лет, при этом у подавляющего большинства пациентов имеет место ожирение и другие компоненты метаболического синдрома (см. п. 11.2). Пациенты не предъявляют жалоб на снижение работоспособности, если для этого отсутствуют другие причины. Жалобы на жажду и полиурию редко достигают значительной выраженности. Достаточно часто пациентов беспокоит кожный и влагалищный зуд, в связи с чем они обращаются к дерматологам и гинекологам. Поскольку от реальной манифестации СД-2 до постановки диагноза зачастую проходят многие годы (в среднем около 7 лет), у многих пациентов на момент выявления заболевания в клинической картине доминируют симптомы и проявления поздних осложнений СД. Более того, первое обращение пациента с СД-2 за медицинской помощью очень часто происходит в связи с поздними осложнениями. Так, пациенты могут госпитализироваться в хирургические стационары с язвенным поражением ног (синдром диабетической стопы), обращаться в связи с прогрессирующим снижением зрения к офтальмологам (диабетическая ретинопатия), госпитализироваться с инфарктами, инсуль-
тами, облитерирующим поражением сосудов ног в учреждения, где у них впервые обнаруживается гипергликемия.
Диагностика
Критерии диагностики, единые для всех типов СД, представлены в п. 7.3. Диагноз СД-2 в подавляющем большинстве случаев базируется на выявлении гипергликемии у лиц с типичными клиническими признаками СД-2 (ожирение, возраст старше 40-45 лет, положительный семейный анамнез СД-2, другие компоненты метаболического синдрома), при отсутствии клинических и лабораторных признаков абсолютного дефицита инсулина (выраженное похудение, кетоз). Сочетание высокой распространенности СД-2, свойственного ему длительного бессимптомного течения и возможности предотвращения его тяжелых осложнений при условии ранней диагностики предопределяют необходимость скрининга, т.е. проведения обследования с целью исключения СД-2 среди лиц без каких-либо симптомов заболевания. Основным тестом, как указывалось, является определение уровня гликемии натощак. Оно показано в следующих ситуациях:
1. У всех людей в возрасте старше 45 лет, особенно при избытке массы тела (ИМТ более 25 кг/м 2) с интервалом раз в 3 года.
2. В более молодом возрасте при наличии избытка массы тела (ИМТ более 25 кг/м 2) и дополнительных факторов риска, к которым относятся:
Малоподвижный образ жизни;
СД-2 у ближайших родственников;
Принадлежность к национальностям высокого риска развития СД-2 (афроамериканцы, латиноамериканцы, коренные американцы и др.);
Женщины, родившие ребенка весом более 4 кг и/или при наличии гестационного СД в анамнезе;
Артериальная гипертензия (≥ 140/90 мм Hg);
Уровень ЛПВП > 0,9 ммоль/л и/или триглицеридов > 2,8 ммоль/л;
Синдром поликистозных яичников;
НТГ и НГНТ;
Сердечно-сосудистые заболевания.
Значительный рост заболеваемости СД-2 среди детей диктует необходимость скринингового определения уровня гликемии среди детей и подростков (начиная с 10 лет с интервалом в 2 года или с началом
пубертата, если он произошел в более раннем возрасте), относящихся к группам повышенного риска, к которым относятся дети с избытком массы тела (ИМТ и/или масса тела > 85 перцентиля, соответствующего возрасту, или вес более 120 % по отношению к идеальному) в сочетании с любыми двумя перечисленными дополнительными факторами риска:
СД-2 среди родственников первой или второй линии родства;
Принадлежность к национальностям высокого риска;
Клинические проявления, ассоциированные с инсулинорезистентностью (acanthosis nigricans, артериальная гипертензия, дислипидемия);
СД, в том числе гестационный, у матери.
Дифференциальная диагностика
Наибольшее клиническое значение имеет дифференциальная диагностика СД-2 и СД-1, принципы которой описаны в п. 7.5 (табл. 7.6). Как указывалось, в большинстве случаев она базируется на данных клинической картины. В тех случаях, когда установление типа СД встречает затруднения, или есть подозрение на какой-то редкий вариант СД, в том числе в рамках наследственных синдромов, наиболее важный практический вопрос, на который необходимо ответить, состоит в том, нуждается ли пациент в инсулинотерапии.
Лечение
Основными компонентами лечения СД-2 являются: диетотерапия, расширение физической активности, сахароснижающая терапия, профилактика и лечение поздних осложнений СД. Поскольку большинство пациентов с СД-2 страдают ожирением, диета должна быть направлена на снижение веса (гипокалорийная) и профилактику поздних осложнений, в первую очередь макроангиопатии (атеросклероза). Гипокалорийная диета необходима всем пациентам с избытком массы тела (ИМТ 25-29 кг/м 2) или ожирением (ИМТ > 30 кг/м 2). В большинстве случаев следует рекомендовать снижение суточного калоража пищи до 1000-1200 ккал для женщин и до 1200-1600 ккал для мужчин. Рекомендуемое соотношение основных пищевых компонентов при СД-2 аналогично таковому при СД-1 (углеводы - 65 %, белки 10-35 %, жиры до 25-35 %). Употребление алкоголя необходимо ограничить в связи с тем, что он является существенным источником дополнительных калорий, кроме того, прием алкоголя на фоне тера-
пии препаратами сульфонилмочевины и инсулином может спровоцировать развитие гипогликемии (см. п. 7.7.3).
Рекомендации по расширению физической активности должны быть индивидуализированы. В начале рекомендуются аэробные нагрузки (ходьба, плаванье) умеренной интенсивности продолжительностью 30-45 минут 3-5 раз в день (около 150 минут в неделю). В дальнейшем необходимо постепенное увеличение физических нагрузок, что в существенной мере способствует снижению и нормализации массы тела. Кроме того, физические нагрузки способствуют снижению инсулинорезистентности и оказывают гипогликемизирующее действие. Сочетание диетотерапии и расширения физических нагрузок без назначения сахароснижающих препаратов позволяет поддерживать компенсацию СД в соответствии с установленными целями (табл. 7.3) примерно у 5 % пациентов с СД-2.
Препараты для сахароснижающей терапии при СД-2 могут быть подразделены на четыре основные группы.
I. Препараты, способствующие снижению инсулинорезистентности (сенситайзеры). К этой группе относится метформин и тиазолидиндионы. Метформин является единственным использующимся в настоящее время препаратом из группы бигуанидов. Основными компонентами механизма его действия являются:
1. Подавление глюконеогенеза в печени (снижение продукции глюкозы печенью), которое приводит к снижению уровня гликемии натощак.
2. Снижение инсулинорезистентности (увеличение утилизации глюкозы периферическими тканями, прежде всего мышцами).
3. Активация аннаэробного гликолиза и уменьшение всасывания глюкозы в тонкой кишке.
Метформин является препаратом первого выбора сахароснижающей терапии у пациентов с СД-2, ожирением и гипергликемией натощак. Начальная доза составляет 500 мг на ночь или во время ужина. В дальнейшем доза постепенно повышается до 2-3 грамм на 2-3 приема. Среди побочных эффектов относительно часто встречаются диспепсические явления (диарея), которые, как правило, транзиторны и проходят самостоятельно через 1-2 недели приема препарата. Поскольку метформин не оказывает стимулирующего эффекта на продукцию инсулина, на фоне монотерапии этим препаратом гипогликемии не
развиваются (его действие обозначатся как антигипергликемическое, а не как гипогликемическое). Противопоказаниями к назначению метформина являются беременность, тяжелая сердечная, печеночная, почечная и другая органная недостаточность, а также гипоксические состояния другого генеза. Крайне редким осложнением, которое встречается при назначении метформина без учета приведенных противопоказаний, является лактатацидоз, являющийся следствием гиперактивации анаэробного гликолиза.
Тиазолидиндионы (пиоглитазон, розиглитазон) являются агонистами γ-рецепторов, активируемых пролифератором пероксисом (PPAR-γ). Тиазолидиндионы активируют метаболизм глюкозы и липидов в мышечной и жировой тканях, что приводит к повышению активности эндогенного инсулина, т.е. К устранению инсулинорезистентности (сенситайзеры инсулина). Суточная доза пиоглитазона составляет 15-30 мг/сут, розиглитазона - 4-8 мг (на 1-2 приема). Весьма эффективна комбинация тиазолидиндионов с метформином. Противопоказанием к назначению тиазолидиндионов является повышение (в 2,5 раза и более) уровня печеночных трансаминаз. Помимо гепатотоксичности, к побочным эффектам тиазолидиндионов относятся задержка жидкости и отеки, которые чаще развиваются при комбинации препаратов с инсулином.
II. Препараты, воздействующие на β-клетку и способствующие усилению секреции инсулина. К этой группе относятся препараты сульфонилмочевины и глиниды (прандиальные регуляторы гликемии), которые используют преимущественно для нормализации уровня гликемии после еды. Основной мишенью препаратов сульфонилмочевины (ПСМ) являются β-клетки панкреатических островков. ПСМ связываются на мембране β-клеток со специфическими рецепторами. Это приводит к закрытию АТФ-зависимых калиевых каналов и деполяризации клеточной мембраны, что в свою очередь способствует открытию кальциевых каналов. Поступление кальция внутрь β -клеток приводит к их дегрануляции и выбросу инсулина в кровь. В клинической практике используется достаточно много ПСМ, которые отличаются по продолжительности и выраженности сахароснижающего эффекта (табл. 7.9).
Табл. 7.9. Препараты сульфонилмочевины
 Основным
и достаточно частым побочным эффектом ПСМ является гипогликемия (см. п.
7.7.3). Она может возникать при передозировке препаратом, его кумуляции
(почечная недостаточность),
Основным
и достаточно частым побочным эффектом ПСМ является гипогликемия (см. п.
7.7.3). Она может возникать при передозировке препаратом, его кумуляции
(почечная недостаточность),
несоблюдении диеты (пропуск приема пищи, прием алкоголя) или режима (значительная физическая нагрузка, перед которой не снижена доза ПСМ или не приняты углеводы).
К группе глинидов (прандиальные регуляторы гликемии) относятся репаглинид (производное бензоевой кислоты; суточная доза 0,5-16 мг/сут) и натеглинид (производное D-фенилаланина; суточная доза 180-540 мг/сут). После приема препараты быстро и обратимо взаимодействуют с рецептором сульфонилмочевины на β-клетке, в результате чего происходит короткое повышение уровня инсулина, которое имитирует первую фазу его секреции в норме. Препараты принимаются за 10-20 минут до основных приемов пищи, обычно 3 раза в день.
III. Препараты, снижающие всасывание глюкозы в кишечнике.
К этой группе относится акарбоза и гуаровая смола. Механизм действия акарбозы заключается в обратимой блокаде α-гликозидаз тонкой кишки, в результате которой замедляются процессы последовательного ферментирования и всасывания углеводов, снижается скорость резорбции и поступления глюкозы в печень и снижается уровень постпрандиальной гликемии. Начальная доза акарбозы составляет 50 мг 3 раза в день, в дальнейшем доза может быть увеличена до 100 мг 3 раза в сутки; препарат принимается непосредственно перед едой или во время еды. Основным побочным эффектом акарбозы является кишечная диспепсия (диареи, метеоризм), которая связана с поступлением невсосавшихся углеводов в толстую кишку. Сахароснижающий эффект акарбозы весьма умерен (табл. 7.10).
В клинической практике таблетированные сахароснижающие препаратов эффективно комбинируется друг с другом и с препаратами инсулина, поскольку у большинства пациентов одновременно определяется как тощаковая, так и постпрандиальная гипергликемия. Существуют многочисленные фиксированные комбинации препаратов в одной таблетке. Наиболее часто в одной таблетке комбинируют метформин с различными ПСМ, а также метформин с тиазолидиндионами.
Табл. 7.10. Механизм действия и потенциальная эффективность таблетированных сахароснижающих препаратов
 IV. Инсулины и аналоги инсулинов
IV. Инсулины и аналоги инсулинов
На определенном этапе препараты инсулинов начинают получать до 30-40 % пациентов с СД-2. Показания для инсулинотерапии при СД-2 приведены в начале п. 7.4. Наиболее частый вариант перевода пациентов с СД-2 на инсулинотерапию заключается в назначении инсулина пролонгированного действия (инсулин НПХ, гларгин или детемир) в комбинации с принимаемыми таблетированными сахароснижающими препаратами. В ситуации, когда уровень гликемии натощак не удается контролировать назначением метформина или последний противопоказан, пациенту назначается вечерняя (на ночь) инъекция инсулина. При невозможности контролировать при помощи таблетированных препаратов как тощаковую, так и постпрандиальную гликемию, пациент переводится на моноинсулинотерапию. Обычно, при СД-2 инсулинотерапия ведется по так называемой «традиционной» схеме, которая подразумевает назначение фиксированных доз инсулина пролонгированного и короткого действия. В этом плане
удобны стандартные смеси инсулинов, содержащие в одном флаконе инсулин короткого (ультракороткого) и пролонгированного действия. Выбор традиционной инсулинотерапии определяется тем, что при СД-2 она зачастую назначается пожилым пациентам, обучение которых самостоятельному изменению дозы инсулина затруднено. Кроме того, интенсивная инсулинотерапия, целью которой является поддержание компенсации углеводного обмена на уровне, приближающемся к нормогликемии, несет повышенный риск гипогликемий. Если для молодых пациентов легкие гипогликемии не представляют серьезной опасности, у пожилых пациентов со сниженным порогом ощущения гипогликемии они могут иметь весьма неблагоприятные последствия со стороны сердечно-сосудистой системы. Молодым пациентам с СД-2, а также пациентам перспективным в плане возможности эффективного обучения, может быть назначен интенсивный вариант инсулинотерапии.
Прогноз
Основной причиной инвалидизации и смерти пациентов с СД-2 являются поздние осложнения (см. п. 7.8), чаще всего диабетическая макроангиопатия. Риск развития отдельных поздних осложнений определяется комплексом факторов, которые обсуждаются в соответствующих главах. Универсальным фактором риска их развития является хроническая гипергликемия. Так, снижение уровня HbA1c у пациентов с СД-2 на 1 % приводит к уменьшению общей смертности примерно на 20 %, на 2 % и 3 % - соответственно примерно на 40 %
7.7. ОСТРЫЕ ОСЛОЖНЕНИЯ САХАРНОГО ДИАБЕТА
7.7.1. Диабетический кетоацидоз
Диабетический кетоацидоз (ДКА) - декомпенсация СД-1, обусловленная абсолютным дефицитом инсулина, при отсутствии своевременного лечения заканчивающаяся кетоацидотической комой (КК) и смертью.
Этиология
Причиной ДКА является абсолютный дефицит инсулина. Той или иной выраженности ДКА определяется у большинства пациентов на момент манифестации СД-1 (10-20 % всех случаев ДКА).
У пациента с установленным диагнозом СД-1 ДКА может развиться при прекращении введения инсулина, зачастую самим пациентом (13 % случаев ДКА), на фоне сопутствующих заболеваний, в первую очередь, инфекционных, при отсутствии увеличения дозы инсулина
Табл. 7.11. Диабетический кетоацидоз
 До
20 % случаев развития ДКА у молодых пациентов с СД-1 связаны с
психологическими проблемами и/или нарушениями пищевого поведения (боязнь
прибавки веса, боязнь гипогликемий, подростковые проблемы). Достаточно
частой причиной ДКА в ряде стран является
До
20 % случаев развития ДКА у молодых пациентов с СД-1 связаны с
психологическими проблемами и/или нарушениями пищевого поведения (боязнь
прибавки веса, боязнь гипогликемий, подростковые проблемы). Достаточно
частой причиной ДКА в ряде стран является
отмена инсулина самим пациентом из-за дороговизны препаратов для некоторых слоев населения (табл. 7.11).
Патогенез
В основе патогенеза ДКА лежит абсолютный дефицит инсулина в сочетании с повышением продукции контринсулярных гормонов, таких как глюкагон, катехоламины и кортизол. В результате происходит значительное усиление продукция глюкозы печенью и нарушение ее утилизации периферическими тканями, нарастание гипергликемии и нарушение осмолярности внеклеточного пространства. Дефицит инсулина в сочетании с относительным избытком контринсулярных гормонов при ДКА приводит к высвобождению в циркуляцию свободных жирных кислот (липолиз) и их несдерживаемому окислению в печени до кетоновых тел (β-гидроксибутират, ацетоацетат, ацетон), в результате чего развивается гиперкетонемия, а в дальнейшем метаболический ацидоз. В результате выраженной глюкозурии развивается осмотический диурез, обезвоживание, потеря натрия, калия и других электролитов (рис. 7.9).
Эпидемиология
Частота новых случаев ДКА составляет 5-8 на 1000 пациентов с СД-1 в год и напрямую зависит от уровня организации медицинской помощи больным СД. Ежегодно в США происходит около 100 000 госпитализаций по поводу ДКА, при этом с учетом затраты на одного пациента за госпитализацию 13 тыс. долларов, ежегодно на стационарное лечение ДКА тратится более 1 миллиарда долларов в год. В РФ в 2005 г. ДКА зафиксирован у 4,31 % детей, 4,75 % подростков и 0,33 % взрослых пациентов с СД-1.
Клинические проявления
Развитие ДКА в зависимости от вызвавшей его причины может занимать от нескольких недель до суток. В большинстве случаев ДКА предшествуют симптомы декомпенсации диабета, но иногда они могут не успеть развиться. Клинические симптомы ДКА включают полиурию, полидипсию, похудение, разлитые боли в животе («диабетический псевдоперитонит»), дегидратацию, выраженную слабость, запах ацетона изо рта (или фруктовый запах), постепенное помутнение сознания. Истинная кома при ДКА в последнее время в силу ранней диагностики развивается относительно редко. При физикальном исследовании выявляются признаки обезвоживания: снижение
 Рис. 7.9. Патогенез кетоацидотической комы
Рис. 7.9. Патогенез кетоацидотической комы
тургора кожи и плотности глазных яблок, тахикардия, гипотония. В далеко зашедших случаях развивается дыхание Куссмауля. Более чем у 25 % пациентов с ДКА развивается рвота, которая по цвету может напоминать кофейную гущу.
Диагностика
Базируется на данных клинической картины, указаниях на наличие у пациента СД-1, а также данных лабораторного исследования. Для ДКА характерна гипергликемия (в ряде случаев незначительная), кетонурия, метаболический ацидоз, гиперосмолярность (табл. 7.12).
Табл. 7.12. Лабораторная диагностика острых осложнений сахарного диабета
 При
обследовании пациентов с острой декомпенсацией СД необходимо
определение уровня гликемии, креатинина и мочевины, электролитов, на
основании чего производится расчет эффективной осмолярности. Кроме того,
необходима оценка кислотно-основного состояния. Эффективная осмолярность
(ЭО) рассчитывается по следующей формуле: 2 *. В норме ЭО составляет 285 - 295 мОсм/л.
При
обследовании пациентов с острой декомпенсацией СД необходимо
определение уровня гликемии, креатинина и мочевины, электролитов, на
основании чего производится расчет эффективной осмолярности. Кроме того,
необходима оценка кислотно-основного состояния. Эффективная осмолярность
(ЭО) рассчитывается по следующей формуле: 2 *. В норме ЭО составляет 285 - 295 мОсм/л.
У большинства пациентов с ДКА определяется лейкоцитоз, выраженность которого пропорциональна уровню кетоновых тел в крови. Уровень натрия, как правило, снижен вследствие осмотического оттока жидкости из интрацеллюлярных пространств в экстрацеллюлярные в ответ на гипергликемию. Реже уровень натрия может быть снижен ложноположительно как следствие выраженной гипер-
триглицеридемии. Уровень калия сыворотки исходно может быть повышен вследствие его перемещения из экстрацеллюлярных пространств.
Дифференциальная диагностика
Другие причины потери сознания у пациентов с СД. Дифференциальная диагностика с гиперосмолярной комой, как правило, не вызывает затруднений (развивается у пожилых пациентов с СД-2) и не имеет большого клинического значения, т.к. принципы лечения обоих состояний сходны. При невозможности оперативно выяснить причину потери сознания пациента с СД ему показано введение глюкозы, т.к. гипогликемические состояния встречаются значительно чаще, а быстрая положительная динамика на фоне введения глюкозы сама по себе позволяет выяснить причину потери сознаний.
Лечение
Лечение ДКА подразумевает регидратацию, коррекцию гипергликемии, электролитных расстройств, а также лечение заболеваний, вызвавших декомпенсацию диабета. Лечение наиболее оптимально проводить в реанимационном отделении специализированного лечебного учреждения. У взрослых пациентов без тяжелой сопутствующей сердечной патологии еще на догоспитальном этапе в качестве первоочередной меры с целью регидратации рекомендуется введение изотонического раствора (0,9 % NaCl) ориентировочно со скоростью литр в час (около 15-20 мл на килограмм веса в час). Полное возмещение дефицита жидкости, которое при ДКА составляет 100-200 мл на кг веса, должно быть достигнуто в пределах первых суток лечения. При сопутствующей сердечной или почечной недостаточности этот период времени должен быть увеличен. Для детей рекомендуемый объем изотонического раствора для регидратационной терапии составляет 10-20 мл на кг массы тела в час, при этом за первые 4 часа он не должен превысить 50 мл на кг веса. Полную регидратацию рекомендуется достигнуть примерно через 48 часов. После того как на фоне параллельно проводимой инсулинотерапии уровень гликемии снизится примерно до 14 ммоль/л, переходят на переливание 10 % раствора глюкозы, которым и продолжается регидратация.
В настоящее время принята концепция «малых доз» инсулина при лечении ДКА. Используется только инсулин короткого действия. Наиболее оптимально использование внутривенного введения инсу-
лина. Внутримышечное введение инсулина, которое менее эффективно, возможно только при умеренной тяжести ДКА, при стабильной гемодинамике и при невозможности проведения внутривенной терапии. В последнем случае инъекции делаются в прямую мышцу живота, при этом на инсулиновый шприц надевается игла для внутримышечных инъекций (для надежного внутримышечного попадания), и по этой игле инсулин набирается из флакона в шприц.
Возможно несколько вариантов внутривенного введения инсулина. Во-первых, инсулин может вводиться «в резинку» инфузионной системы, при этом необходимое количество инсулина набирается в инсулиновый шприц, после чего в него добирается 1 мл изотонического раствора. Вплоть до достижения уровнем гликемии 14 ммоль/л ежечасно пациенту вводится по 6-10 Ед инсулина короткого действия; в дальнейшем (параллельно со сменой регидратационного раствора с изотонического на 10 % глюкозу) в зависимости от ежечасно определяемых показателей гликемии доза инсулина снижается до 4-8 Ед в час. Рекомендованная скорость снижения уровня гликемии не должна превышать 5 ммоль/л в час. Другой вариант внутривенной инсулинотерапии подразумевает использование перфузора. Для приготовления раствора для перфузора исходят из соотношения: к 50 Ед инсулина короткого действия добавляется 2 мл 20 % раствора альбумина человека, после чего добавляется 50 мг 0,9 % изотонического раствора. В случае, если выбран внутримышечный путь введения инсулина, исходно вводится 20 Ед инсулина короткого действия, после чего ежечасно по 6 Ед, а после достижения уровнем гликемии 14 ммоль/л доза снижается до 4 Ед в час. После полной стабилизации гемодинамики и компенсации кислотно-основных нарушений пациент переводится на подкожные инъекции инсулина.
Как указывалось, несмотря на значительный дефицит калия в организме (общая потеря 3-6 ммоль/кг), при ДКА его уровень до начала инсулинотерапии может быть несколько повышен. Тем не менее, начало переливания раствора хлорида калия рекомендуется проводить одновременно с началом инсулинотерапии, если уровень калия плазмы меньше 5,5 ммоль/л. Успешная коррекция дефицита калия происходит только на фоне нормализации рН. При низком рН поступление калия внутрь клетки значительно снижено, в связи с этим, по возможности дозу переливаемого хлорида калия желательно адаптировать к конкретному показателю рН (табл. 7.13).
Табл. 7.13. Схема коррекции дефицита калия
 * Для расчета используют следующие данные:
* Для расчета используют следующие данные:
1 г KCl = 13,4 ммоль; 1 ммоль KCl = 0,075 г. В 4% раствор КС1: в 100 мл - 4 г КС1, в 25 мл - 1 г КС1, в 10 мл 0,4 г КС1.
Причиной декомпенсации диабета зачастую являются инфекционные заболевания (пиелонефрит, инфицированная язва при синдроме диабетической стопы, пневмония, синусит и проч.). Существует правило, согласно которому при ДКА антибиотикотерапия назначается практически всем пациентам с субфебрилитетом или лихорадкой даже при отсутствии видимого очага инфекции, поскольку собственно для ДКА повышение температуры тела не характерно.
Прогноз
Смертность при ДКА составляет 0,5-5 %, при этом большинство случаев обусловлено поздним и неквалифицированным оказанием медицинской помощи. Смертность наиболее высока (до 50 %) среди пациентов пожилого возраста.
7.7.2. Гиперосмолярная кома
Гиперосмолярная кома (ГОК) - редкое острое осложнение СД-2, развивающееся вследствие выраженной дегидратации и гипергликемии на фоне отсутствия абсолютного дефицита инсулина, сопровождающееся высокой летальностью (табл. 7.14).
Этиология
ГОК, как правило, развивается у пожилых пациентов с СД-2. Такие пациенты чаще всего одиноки, живут без ухода, пренебрегают своим состоянием и самоконтролем и принимают недостаточно жидкости. Часто к декомпенсации приводят инфекции (синдром диабетической стопы, пневмонии, острый пиелонефрит), нарушения мозгового
кровообращения и другие состояния, в результате которых пациенты плохо передвигаются, не принимают сахароснижающие препараты и жидкость.
Табл. 7.14. Гиперосмолярная кома (ГОК)
 Патогенез
Патогенез
Нарастающая гипергликемия и осмотический диурез обусловливают выраженную дегидратацию, которая по указанным выше причинам не восполняется извне. Результатом гипергликемии и дегидратации является гиперосмолярность плазмы. Неотъемлемым компонентом патогенеза ГОК является относительный дефицит инсулина и избыток контринсулярных гормонов, тем не менее, сохраняющейся при СД-2 остаточной секреции инсулина оказывается достаточно для подавления липолиза и кетогенеза, вследствие чего не происходит развития кетоацидоза.
В ряде случаев может определяться умеренной выраженности ацидоз как результат гиперлактатемии на фоне тканевой гипоперфузии. При выраженной гипергликемии для сохранения осмотического баланса в цереброспинальной жидкости увеличивается содержание натрия, поступающего из клеток головного мозга, куда в обмен попадает калий. Нарушается трансмембранный потенциал нервных клеток. Развивается прогрессирующее помрачение сознания в сочетании с судорожным синдромом (рис. 7.10).
Эпидемиология
На ГОК приходится 10-30 % острых гипергликемических состояний у взрослых и пожилых пациентов с СД-2. Примерно в 2 / 3 случаев ГОК развивается у лиц с недиагностированным до этого СД.
Клинические проявления
Особенностями клинической картины гиперосмолярной комы являются:
Комплекс признаков и осложнений дегидратации и гипоперфузии: жажда, сухость слизистых, тахикардия, артериальная гипотензия, тошнота, слабость, шок;
Фокальные и генерализованные судороги;
Лихорадка, тошнота и рвота (40-65 % случаев);
Из сопутствующих заболеваний и осложнений часто встречаются тромбозы глубоких вен, пневмония, нарушения мозгового кровообращения, гастропарез.
Диагностика
Базируется на данных клинической картины, возрасте пациента и анамнезе СД-2, выраженной гипергликемии при отсутствии кетонурии и кетоацидоза. Типичные лабораторные признаки ГОК представлены в табл. 7.12.
 Рис. 7.10.
Патогенез гиперосмолярной комы
Рис. 7.10.
Патогенез гиперосмолярной комы
Дифференциальная диагностика
Другие острые состояния, развивающиеся у пациентов с СД, чаще всего с сопутствующей патологией, приведшей к выраженной декомпенсации СД.
Лечение
Лечение и мониторинг при ГОК, за исключением некоторых особенностей, не отличаются от таковых, описанных для кетоацидотической диабетической комы (п. 7.7.1):
Больший объем начальной регидратации 1,5-2 л за 1-й час; 1 л - за 2-й и 3-й час, далее по 500 мл/ч изотонического раствора хлорида натрия;
Потребность во введении калийсодержащих растворов, как правило, больше, чем при кетоацидотической коме;
Инсулинотерапия аналогична таковой при КК, но потребность в инсулине меньше и уровень гликемии необходимо снижать не быстрее, чем на 5 ммоль/л в час во избежание развития отека мозга;
Введения гипотонического раствора (NaCl 0,45 %) лучше избегать (только при выраженной гипернатриемии: > 155 ммоль/л и/или эффективной осмолярности > 320 мОсм/л);
Во введении бикарбоната нет необходимости (только в специализированных реанимационных отделениях при ацидозе с рН < 7,1).
Прогноз
Летальность при ГОК высока и составляет 15-60 %. Наихудший прогноз у пожилых пациентов с тяжелой сопутствующей патологией, которая, зачастую, и является причиной декомпенсации СД и развития ГОК.
7.7.3. Гипогликемия
Гипогликемия - снижение уровня глюкозы в сыворотке крови (<2,2- 2,8 ммоль/л), сопровождающее клинический синдром, характеризующийся признаками активации симпатической нервной системы и/или дисфункцией центральной нервной системы. Гипогликемия как лабораторный феномен не тождественен понятию «гипогликемическая симптоматика», поскольку лабораторные данные и клиническая картина не всегда совпадают.
Этиология
Передозировка препаратов инсулина и его аналогов, а также препаратов сульфонилмочевины;
Недостаточный прием пищи на фоне неизменной сахароснижающей терапии;
Прием алкогольных напитков;
Физические нагрузки на фоне неизменной сахароснижающей терапии и/или без дополнительного приема углеводов;
Развитие поздних осложнений СД (автономная нейропатия с гастропарезом, почечная недостаточность) и ряда других заболеваний (надпочечниковая недостаточность, гипотиреоз, печеночная недостаточность, злокачественные опухоли) при неизменной сахароснижающей терапии (продолжение приема и кумуляция ТСП на фоне почечной недостаточности, сохранение прежней дозы инсулина);
Нарушение техники введения инсулина (внутримышечная инъекция вместо подкожной);
Артифициальная гипогликемия (сознательная передозировка сахароснижающих препаратов самим пациентом);
Органический гиперинсулинизм - инсулинома (см. п. 10.3).
Патогенез
Патогенез гипогликемии заключается в нарушении баланса между поступлением глюкозы в кровь, ее утилизацией, уровнем инсулина и контринсулярных гормонов. В норме при уровне гликемии в пределах 4,2-4,7 ммоль/л продукция и высвобождение инсулина из β-клеток подавлены. Снижение уровня гликемии менее 3,9 ммоль/л сопровождается стимуляцией продукции контринсулярных гормонов (глюкагон, кортизол, гормон роста, адреналин). Нейрогликопеническая симптоматика развивается при снижении уровня гликемии менее 2,5-2,8 ммоль/л. При передозировке инсулином и/или препаратами сульфонилмочевины гипогликемия развивается вследствие прямого гипогликемизирующего действия экзогенного или эндогенного гормона. В случае передозировки препаратами сульфонилмочевины гипогликемическая симптоматика может многократно рецидивировать после купирования приступа вследствие того, что длительность действия ряда препаратов может достигать суток и более. ТСП, которые не оказывают стимулирующего влияния на продукцию инсулина (метформин, тиазолидиндионы), сами по себе гипогликемии вызвать не могут, но при их добавлении к препаратам сульфонилмочевины или инсулину прием последних в прежней дозе может стать причиной гипогликемии вследствие кумуляции сахароснижающего эффекта комбинированной терапии (табл. 7.15).
Табл. 7.15. Гипогликемия
 Окончание табл. 7.15
Окончание табл. 7.15
 При приеме алкоголя
происходит подавление глюконеогенеза в печени, который является важнейшим фактором, противодействующим гипогликемии. Физические нагрузки
способствуют
инсулиннезависимой утилизации глюкозы, благодаря чему на фоне
неизменной сахароснижающей терапии и/или при отсутствии дополнительного
приема углеводов могут явиться причиной гипогликемии.
При приеме алкоголя
происходит подавление глюконеогенеза в печени, который является важнейшим фактором, противодействующим гипогликемии. Физические нагрузки
способствуют
инсулиннезависимой утилизации глюкозы, благодаря чему на фоне
неизменной сахароснижающей терапии и/или при отсутствии дополнительного
приема углеводов могут явиться причиной гипогликемии.
Эпидемиология
Легкие, быстро купирующиеся гипогликемии у пациентов с СД-1, получающих интенсивную инсулинотерапию, могут развиваться несколько раз в неделю, и относительно безвредны. На одного больного, находящегося на интенсивной инсулинотерапии, в год приходится 1 случай тяжелой гипогликемии. В большинстве случаев гипогликемии развиваются в ночное время. При СД-2 у 20 % пациентов, получающих инсулин, и у 6 %, получающих препараты сульфонилмочевины, на протяжении 10 лет развивается как минимум один эпизод тяжелой гипогликемии.
Клинические проявления
Выделяют две основные группы симптомов: адренергические, связанные с активацией симпатической нервной системы и выбросом адреналина надпочечниками, и нейрогликопенические, связанные с нарушением функционирования центральной нервной системы на фоне дефицита ее основного энергетического субстрата. К адренергическим симптомам относятся: тахикардия, мидриаз; беспокойство, агрессивность; дрожь, холодный пот, парестезии; тошнота, сильный голод, гиперсаливация; диарея, обильное мочеиспускание. К нейрогликопеническим симптомам относят астению,
снижение концентрации внимания, головную боль, чувство страха, спутанность сознания, дезориентацию, галлюцинации; речевые, зрительные, поведенческие нарушения, амнезию, нарушение сознания, судороги, преходящие параличи, кому. Четкой зависимости выраженности и последовательности развития симптомов по мере утяжеления гипогликемии может не быть. Могут возникать только адренергические или только нейрогликопенические симптомы. В отдельных случаях, несмотря на восстановление нормогликемии и продолжающуюся терапию, пациенты могут пребывать в ступорозном или даже коматозном состоянии на протяжении нескольких часов и даже дней. Длительная гипогликемия или ее частые эпизоды могут привести к необратимым изменениям в ЦНС (прежде всего в коре больших полушарий), проявления которых значительно варьируют от делириозных и галлюцинаторно-параноидных эпизодов до типичных эпилептических припадков, неизбежным исходом которых является стойкое слабоумие.
Гипергликемия субъективно переносится пациентами легче, чем эпизоды даже легкой гипогликемии. Поэтому многие пациенты из-за боязни гипогликемии считают необходимым поддержание гликемии на относительно высоком уровне, который фактически соответствует декомпенсации заболевания. Преодоление этого стереотипа требует порой немалых усилий врачей и обучающего персонала.
Диагностика
Клиническая картина гипогликемии у пациента с СД в сочетании с лабораторным (как правило, при помощи глюкометра) выявлением низкого уровня глюкозы крови.
Дифференциальная диагностика
Другие причины, приводящие к потере сознания. Если причина потери сознания больного СД неизвестна и невозможно проведение экспресс-анализа уровня гликемии, ему показано введение глюкозы. Нередко возникает необходимость выяснения причины развития частых гипогликемий у пациентов с СД. Наиболее часто они являются следствием неадекватной сахароснижающей терапии и низкого уровня знаний пациента о своем заболевании. Следует помнить о том, что к снижению потребности в сахароснижающей терапии вплоть до ее полной отмены («исчезнувший СД») могут приводить ряд заболеваний (надпочечниковая недостаточность, гипотиреоз, почечная и печеночная недостаточность), в том числе злокачественные опухоли.
Лечение
Для лечения легкой гипогликемии, при которой пациент в сознании и может сам оказать себе помощь, обычно достаточно принять пищу или жидкость, содержащую углеводы в количестве 1-2 хлебных единиц (10-20 г глюкозы). Такое количество содержится, например, в 200 мл сладкого фруктового сока. Напитки более эффективно купируют гипогликемию, поскольку в жидком виде глюкоза значительно скорее всасывается. Если симптоматика продолжает нарастать, несмотря на продолжающийся прием углеводов, необходимо внутривенное введение глюкозы или внутримышечное глюкагона. Аналогичным образом лечится и тяжелая гипогликемия, протекающая с потерей сознания. В этом случае пациенту вводится около 50 мл 40 % раствора глюкозы внутривенно. Введение глюкозы необходимо продолжать вплоть до купирования приступа и нормализации гликемии, хотя большей дозы - до 100 мл и более, как правило, не требуется. Глюкагон вводится (как правило, приготовленным в заводских условиях наполненным шприцем) внутримышечно или подкожно. Через несколько минут уровень гликемии благодаря индукции глюкагоном гликогенолиза нормализуется. Однако это происходит не всегда: при высоком уровне инсулина в крови глюкагон неэффективен. Период полувыведения глюкагона короче, чем инсулина. При алкоголизме и болезнях печени синтез гликогена нарушен, и введение глюкагона может оказаться неэффективным. Побочным эффектом введения глюкагона может быть рвота, создающая опасность аспирации. Близким пациента желательно владеть техникой инъекции глюкагона.
Прогноз
Легкие гипогликемии у обученных пациентов на фоне хорошей компенсации заболевания безопасны. Частые гипогликемии являются признаком плохой компенсации СД; в большинстве случаев у таких пациентов в остальное время суток определяется более или менее выраженная гипергликемия и высокий уровень гликированного гемоглобина. У пожилых пациентов с поздними осложнениями СД гипогликемии могут провоцировать такие сосудистые осложнения, как инфаркт миокарда, инсульт, кровоизлияние в сетчатку. Гипогликемическая кома длительностью до 30 мин при адекватном лечении и быстром возвращении сознания, как правило, не имеет каких-либо осложнений и последствий.
7.8. ПОЗДНИЕ ОСЛОЖНЕНИЯ САХАРНОГО ДИАБЕТА
Поздние осложнения развиваются при обоих типах СД. Клинически выделяют пять основных поздних осложнений СД: макроангиопатию, нефропатию, ретинопатию, нейропатию и синдром диабетической стопы. Неспецифичность поздних осложнений для отдельных типов СД определяется тем, что их основным патогенетическим звеном является хроническая гипергликемия. В связи с этим на момент манифестации СД-1 поздние осложнения у пациентов практически никогда не встречаются, развиваясь через годы и десятилетия в зависимости от эффективности проводимой терапии. Наибольшее клиническое значение при СД-1, как правило, приобретает диабетическая микроангиопатия (нефропатия, ретинопатия) и нейропатия (синдром диабетической стопы). При СД-2, напротив, поздние осложнения часто выявляются уже на момент установления диагноза. Во-первых, это связано с тем, что СД-2 манифестирует задолго до установления диагноза. Во-вторых, атеросклероз, клинически проявляющийся макроангиопатией, имеет много общих с СД звеньев патогенеза. При СД-2 наибольшее клиническое значение, как правило, приобретает диабетическая макроангиопатия, которая на момент постановки диагноза выявляется у подавляющего большинства пациентов. В каждом конкретном случае набор и выраженность отдельных поздних осложнений варьируют от их парадоксального полного отсутствия, несмотря на значительную длительность заболевания вплоть до сочетания всех возможных вариантов в тяжелой форме.
Поздние осложнения являются основной причиной смерти пациентов с СД, а принимая во внимание его распространенность - важнейшей медико-социальной проблемой здравоохранения большинства стран. В связи с этим основной целью лечения и наблюдения пациентов с СД является профилактика (первичная, вторичная, третичная) его поздних осложнений.
7.8.1. Диабетическая макроангиопатия
Диабетическая макроангиопатия - собирательное понятие, объединяющее атеросклеротическое поражение крупных артерий при СД,
клинически проявляющееся ишемической болезнью сердца (ИБС), облитерирующим атеросклерозом сосудов головного мозга, нижних конечностей, внутренних органов и артериальной гипертензией (табл. 7.16).
Табл. 7.16. Диабетическая макроангиопатия
 Этиология и патогенез
Этиология и патогенез
Вероятно, аналогичны этиологии и патогенезу атеросклероза у лиц без СД. Атеросклеротические бляшки не отличаются по микроскопическому строению у лиц с СД и без него. Тем не менее при СД на первый план могут выступать дополнительные факторы риска, или же СД усугубляет известные неспецифические факторы. К таковым при СД следует отнести:
1. Гипергликемию. Является фактором риска развития атеросклероза. Увеличение уровня HbA1c на 1 % у пациентов с СД-2 увеличива-
ет риск развития инфаркта миокарда на 15 %. Механизм атерогенного действия гипергликемии не вполне ясен, возможно, он связан с гликозированием конечных продуктов метаболизма ЛПНП и коллагена сосудистой стенки.
2. Артериальную гипертензию (АГ). В патогенезе большое значение придается почечному компоненту (диабетическая нефропатия). АГ при СД-2 - не менее значимый фактор риска инфаркта и инсульта, чем гипергликемия.
3. Дислипидемию. Гиперинсулинемия, являющаяся неотъемлемым компонентом инсулинорезистентности при СД-2, обусловливает снижение уровня ЛПВП, повышение уровня триглицеридов и снижение плотности, т.е. усиление атерогенности ЛПНП.
4. Ожирение, которым страдает большинство пациентов с СД-2, является независимым фактором риска атеросклероза, инфаркта миокарда и инсульта (см. п. 11.2).
5. Инсулинорезистентность. Гиперинсулинемия и высокий уровень инсулин-проинсулин-подобных молекул повышает риск развития атеросклероза, что, возможно, связано с эндотелиальной дисфункцией.
6. Нарушение коагуляции крови. При СД определяется повышение уровня фибриногена, активатора ингибитора тромбоцитов и фактора Виллебранда, в результате чего формируется протромботическое состояние свертывающейся системы крови.
7. Эндотелиальную дисфункцию, характеризующуюся повышением экспрессии активатора ингибитора плазминогена и молекул клеточной адгезии.
8. Окислительный стресс, приводящий к повышению концентрации окисленных ЛПНП и F2-изопростанов.
9. Системное воспаление, при котором происходит повышение экспрессии фибриногена и С-реактивного белка.
Наиболее значимыми факторами риска развития ИБС при СД-2 являются повышенный уровень ЛПНП, пониженный ЛПВП, артериальная гипертензия, гипергликемия и курение. Одним из отличий атеросклеротического процесса при СД является более распространенный и дистальный характер окклюзионного поражения, т.е. В процесс чаще вовлекаются относительно более мелкие артерии, что затрудняет хирургическое лечение и ухудшает прогноз.
Эпидемиология
Риск развития ИБС у лиц с СД-2 в 6 раз выше, чем у лиц без диабета, при этом он одинаков для мужчин и женщин. Артериальная гипертензия выявляется у 20 % пациентов с СД-1 и у 75 % с СД-2. В общем, у больных СД она встречается в 2 раза чаще, чем у лиц без него. Облитерирующий атеросклероз периферических сосудов развивается у 10 % больных с СД. Тромбоэмболия сосудов головного мозга развивается у 8 % пациентов с СД (в 2-4 раза чаще, чем у лиц без СД).
Клинические проявления
В основном не отличаются от таковых у лиц без СД. В клинической картине СД-2 макрососудистые осложнения (инфаркт миокарда, инсульт, окклюзионное поражение сосудов ног) зачастую выступают на первый план, и именно при их развитии у пациента нередко впервые обнаруживается гипергликемия. Возможно, вследствие сопутствующей автономной нейропатии до 30 % инфарктов миокарда у лиц с СД протекают без типичного ангинозного приступа (безболевой инфаркт).
Диагностика
Принципы диагностики осложнений атеросклероза (ИБС, нарушение мозгового кровообращения, окклюзионное поражение артерий ног) не отличаются от таковых для лиц без СД. Измерение артериального давления (АД) должно проводиться на каждом визите пациента с СД к врачу, а определение показателей липидного спектра крови (общий холестерин, триглицериды, ЛПНП, ЛПВП) при СД необходимо проводить не реже, чем раз в год.
Дифференциальная диагностика
Другие сердечно-сосудистые заболевания, симптоматическая артериальная гипертензия, вторичные дислипидемии.
Лечение
♦ Контроль артериального давления. Должный уровень систолического АД при СД составляет менее 130 ммHg, а диастолического 80 ммНg (табл. 7.3). Большинству пациентов для достижения этой цели необходимо назначение нескольких гипотензивных препаратов. Препаратами выбора гипотензивной терапии при СД являются ингибиторы АПФ и блокаторы рецепторов ангиотензина, которые при необходимости дополняются тиазидными диуретиками. Препаратами выбора для пациентов с СД, перенесших инфаркт миокарда, являются β-адреноблокаторы.
♦ Коррекция дислипидемии. Целевые уровни показателей липидного спектра представлены в табл. 7.3. Препаратами выбора гиполипидемической терапии являются ингибиторы 3-гидрокси-3-метилглу- тарил-КоА-редуктазы (статины).
♦ Антиагрегантная терапия. Терапия аспирином (75-100 мг/сут) показана пациентам с СД старше 40 лет при повышенном риске развития сердечно-сосудистой патологии (отягощенный семейный анамнез, артериальная гипертензия, курение, дислипидемия, микроальбуминурия), а также всем пациентам с клиническими проявлениями атеросклероза в качестве вторичной профилактики.
♦ Скрининг и лечение ИБС. Нагрузочные тесты для исключения ИБС показаны пациентам с симптомами сердечно-сосудистых заболеваний, а также при выявлении патологии при ЭКГ.
Прогноз
От сердечно-сосудистых заболеваний умирает 75 % пациентов с СД-2 и 35 % пациентов с СД-1. Примерно 50 % больных СД-2 умирают от осложнений ИБС, 15 % от тромбоэмболии сосудов головного мозга. Смертность от инфаркта миокарда у лиц с СД превышает 50 %.
7.8.2. Диабетическая ретинопатия
Диабетическая ретинопатия (ДР) - микроангиопатия сосудов сетчатки глаза, характеризующаяся развитием микроаневризм, кровоизлияний, экссудативных изменений и пролиферацией новообразованных сосудов, приводящая к частичной или полной потере зрения (табл. 7.17).
Этиология
Основным этиологическим фактором развития ДР является хроническая гипергликемия. Другие факторы (артериальная гипертензия, дислипидемия, курение, беременность и др.) имеют меньшее значение.
Патогенез
Основными звеньями патогенеза ДР являются:
Микроангиопатия сосудов сетчатки, приводящая к сужению просвета сосудов с развитием гипоперфузии;
Дегенерация сосудов с образованием микроаневризм;
Прогрессирующая гипоксия, стимулирующая пролиферацию сосудов и приводящая к жировой дистрофии и отложению солей кальция в сетчатке;
Табл. 7.17. Диабетическая ретинопатия
 микроинфаркты с экссудацией, приводящие к образованию мягких «ватных пятен»;
микроинфаркты с экссудацией, приводящие к образованию мягких «ватных пятен»;
Отложение липидов с формированием плотных экссудатов;
Разрастание в сетчатке пролиферирующих сосудов с образованием шунтов и аневризм, приводящих к дилатации вен и усугублению гипоперфузии сетчатки;
Феномен обкрадывания с дальнейшим прогрессированием ишемизации, являющийся причиной образования инфильтратов и рубцов;
Отслоение сетчатки в результате ее ишемической дезинтеграции и образования витреоретинальных тракций;
Кровоизлияния в стекловидное тело в результате геморрагических инфарктов, массивной сосудистой инвазии и разрыва аневризм;
Пролиферация сосудов радужной оболочки (диабетический рубеоз), приводящая к развитию вторичной глаукомы;
Макулопатия с отеком сетчатки.
Эпидемиология
ДР является самой частой причиной слепоты среди трудоспособного населения развитых стран, а риск развития слепоты у пациентов с СД в 10-20 раз выше, чем в общей популяции. На момент диагностики СД-1 ДР не обнаруживается практически ни у кого из пациентов, спустя 5 лет заболевание выявляется у 8 % пациентов, а при тридцатилетнем стаже диабета - у 98 % пациентов. На момент диагностики СД-2 ДР выявляется у 20-40 % пациентов, а среди пациентов с пятнадцатилетнем стажем СД-2 - у 85 %. При СД-1 относительно чаще встречается пролиферативная ретинопатия, а при СД-2 - макулопатия (75 % случаев макулопатии).
Клинические проявления
Согласно общепринятой классификации, выделяют 3 стадии ДР
(табл. 7.18).
Диагностика
Полное офтальмологическое обследование, включающее прямую офтальмоскопию с фотографированием сетчатки, показано пациентам с СД-1 через 3-5 лет после манифестации заболевания, а пациентам с СД-2 - сразу после его выявления. В дальнейшем такие исследования необходимо повторять ежегодно.
Табл. 7.18. Классификация диабетической ретинопатии
 Дифференциальная диагностика
Дифференциальная диагностика
Другие заболевания глаз у пациентов с СД.
Лечение
Базовым принципом лечения диабетической ретинопатии, как и других поздних осложнений, является оптимальная компенсация СД. Наиболее эффективным методом лечения диабетической ретинопатии и предупреждения слепоты является лазерная фотокоагуляция. Целью
 Рис. 7.11.
Диабетическая ретинопатия:
Рис. 7.11.
Диабетическая ретинопатия:
а) непролиферативная; б) препролиферативная; в) пролиферативная
лазерной фотокоагуляции является прекращение функционирования новообразованных сосудов, которые представляют основную угрозу развития таких тяжелых осложнений, как гемофтальм, тракционная отслойка сетчатки, рубеоз радужки и вторичная глаукома.
Прогноз
Слепота регистрируется у 2 % пациентов с СД (3-4 % пациентов с СД- 1 и 1,5-2 % пациентов с СД-2). Примерная частота новых случаев слепоты, связанных с ДР, составляет 3,3 случая на 100000 населения в год. При СД-1 снижение HbA1c до 7,0 % приводит к уменьшению риска развития ДР на 75 % и уменьшению риска прогрессирования ДР на 60 %. При СД-2 снижение HbA1c на 1 % приводит к уменьшению риска развития ДР на 20 %.
7.8.3. Диабетическая нефропатия
Диабетическая нефропатия (ДНФ) определяется как альбуминурия (более 300 мг альбумина в сутки или протеинурия более 0,5 г белка в сутки) и/или снижение фильтрационной функции почек у лиц с СД при отсутствии мочевых инфекций, сердечной недостаточности или других заболеваний почек. Микроальбуминурия определяется как экскреция альбумина 30-300 мг/сут или 20-200 мкг/мин.
Этиология и патогенез
Основными факторами риска ДНФ являются длительность СД, хроническая гипергликемия, артериальная гипертензия, дислипидемия, заболевания почек у родителей. При ДНФ в первую очередь поражается клубочковый аппарат почки.
1. Одним из возможным механизмов, по которому гипергликемия способствует развитию поражения клубочков, является аккумуляция сорбитола за счет активизации полиолового пути метаболизма глюкозы, а также ряда конечных продуктов гликирования.
2. Гемодинамические нарушения, а именно внутриклубочковая артериальная гипертензия (повышение кровяного давления внутри клубочков почки) является важнейшим компонентом патогенеза
Причиной внутриклубочковой гипертензии является нарушение тонуса артериол: расширение приносящей и сужение выносящей.
Табл. 7.19. Диабетическая нефропатия
 Это,
в свою очередь, происходит под воздействием ряда гуморальных факторов,
таких как ангиотензин-2 и эндотелин, а также вследствие нарушения
электролитных свойств базальной мембраны клубочков. Кроме того,
внутриклубочковой гипертензии способствует системная гипертензия,
которая определяется у большинства пациентов с ДНФ. Вследствие
внутриклубочковой гипертензии происходит повреждение базальных мембран и
фильтрационных пор,
Это,
в свою очередь, происходит под воздействием ряда гуморальных факторов,
таких как ангиотензин-2 и эндотелин, а также вследствие нарушения
электролитных свойств базальной мембраны клубочков. Кроме того,
внутриклубочковой гипертензии способствует системная гипертензия,
которая определяется у большинства пациентов с ДНФ. Вследствие
внутриклубочковой гипертензии происходит повреждение базальных мембран и
фильтрационных пор,
через которые начинают проникать следовые (микроальбуминурия), а затем значимые количества альбумина (протеинурия). Утолщение базальных мембран вызывает изменение их электролитных свойств, что само по себе приводит к попаданию большего количества альбумина в ультрафильтрат даже при отсутствии изменения размера фильтрационных пор.
3. Генетическая предрасположенность. У родственников пациентов с ДНФ с повышенной частотой встречается артериальная гипертензия. Существуют данные о связи ДНФ с полиморфизмом гена АПФ. Микроскопически при ДНФ выявляется утолщение базальных мембран клубочков, экспансия мезангия, а также фиброзные изменения приносящих и выносящих артериол. На конечной стадии, которая клинически соответствует хронической почечной недостаточности (ХПН), определяется очаговый (Киммельстиля-Уилсона), а затем диффузный гломерулосклероз.
Эпидемиология
Микроальбуминурия определяется у 6-60 % пациентов с СД-1 спустя 5-15 лет после его манифестации. ДНФ определяется у 35 % с СД-1, чаще у мужчин и у лиц, у которых СД-1 развился в возрасте моложе 15 лет. При СД-2 ДНФ развивается у 25 % представителей европейской расы и у 50 % азиатской расы. Общая распространенность ДНФ при СД-2 составляет 4-30 %.
Клинические проявления
Относительно ранним клиническим проявлением, которое косвенно связано с ДНФ, является артериальная гипертензия. Другие клинически явные проявления относятся к поздним. К ним можно отнести проявления нефротического синдрома и хронической почечной недостаточности.
Диагностика
Скрининг на ДНФ у лиц с СД подразумевает ежегодное тестирование на микроальбуминурию при СД-1 спустя 5 лет после манифестации заболевания, а при СД-2 - сразу после его выявления. Кроме того, необходимо как минимум ежегодное определение уровня креатинина для расчета скорости клубочковой фильтрации (СКФ). СКФ может быть рассчитана при помощи различных формул, например, по формуле Кокрофта-Голта:
Для мужчин: а = 1,23 (норма СКФ 100 - 150 мл/мин) Для женщин: а = 1,05 (норма СКФ 85 - 130 мл/мин)
На начальных стадиях ДНФ может быть выявлено повышение СКФ, которая постепенно падает по мере развития ХПН. Микроальбуминурия начинает определяться через 5-15 лет после манифестации СД-1; при СД-2 в 8-10 % случаев она обнаруживается сразу после его выявления, вероятно, вследствие длительного бессимптомного течения заболевания до постановки диагноза. Пик развития явной протеинурии или альбуминурии при СД-1 приходится между 15 и 20 годами после его начала. Протеинурия свидетельствует о необратимости ДНФ, которая рано или поздно приведет к ХПН. Уремия в среднем развивается через 7-10 лет после появления явной протеинурии. Следует заметить, что СКФ не коррелирует с протеинурией.
Дифференциальная диагностика
Другие причины протеинурии и почечной недостаточности у лиц с СД. В большинстве случаев ДНФ сочетается с артериальной гипертензией, диабетической ретинопатией или нейропатией, при отсутствии которых дифференциальная диагностика должна быть особо тщательной. В 10 % случаев при с СД-1 и в30 % случаев при СД-2 протеинурия не связана с ДНФ.
Лечение
♦ Основными условиями первичной и вторичной профилактики
ДНФ являются компенсация СД и поддержание нормального системного артериального давления. Кроме того, первичная профилактика ДНФ подразумевает уменьшение потребления белковой пищи - менее 35 % суточного калоража.
♦ На стадиях микроальбуминурии и протеинурии пациентам показано назначение ингибиторов АПФ или блокаторов рецепторов ангиотензина. При сопутствующей артериальной гипертензии они назначаются в гипотензивных дозах, при необходимости в комбинации с другими гипотензивными препаратами. При нормальном артериальном давлении эти препараты назначаются в дозах, не приводящих к развитию гипотонии. Как ингибиторы АПФ (при СД-1 и СД-2), так и блокаторы рецепторов ангиотензина (при СД-2) способствуют предотвращению перехода микроальбуминурии в протеинурию. В ряде случаев на фоне указанной терапии в сочетании с компенсацией диабета по другим параметрам микроальбуминурия ликвидируется. Кроме того, начиная со стадии микроальбуминурии необходимо
сокращение потребление белков менее 10 % суточного калоража (или менее 0,8 грамм на кг веса) и соли менее 3 грамм в день.
♦ На стадии ХПН, как правило, требуется коррекция сахароснижающей терапии. Большинство пациентов с СД-2 необходимо перевести на инсулинотерапию, поскольку кумуляция ТСП несет риск развития тяжелой гипогликемии. У большинства пациентов с СД-1 происходит снижение потребности в инсулине, поскольку почка является одним из основных мест его метаболизма. При повышении уровня креатинина сыворотки до 500 мкмоль/л и более необходимо ставить вопрос о подготовке пациента к экстракорпоральному (гемодиализ, перитонеальный диализ) или хирургическому (трансплантация почки) методу лечения. Трансплантация почки показана при уровне креатинина до 600-700 мкмоль/л и снижении скорости клубочковой фильтрации менее 25 мл/мин, гемодиализ - 1000-1200 мкмоль/л и менее 10 мл/мин соответственно.
Прогноз
У 50 % пациентов с СД-1 и 10 % с СД-2, у которых выявляется протеинурия, в течение последующих 10 лет развивается ХПН. 15 % всех смертей пациентов с СД-1 моложе 50 лет связано с ХПН вследствие ДНФ.
7.8.4. Диабетическая нейропатия
Диабетическая нейропатия (ДНЕ) представляет собой сочетание синдромов поражения нервной системы, которые могут быть классифицированы в зависимости от преимущественного вовлечения в процесс ее различных отделов (сенсомоторная, автономная), а также распространенности и тяжести поражения (табл. 7.20).
I. Сенсомоторная нейропатия:
Симметричная;
Фокальная (мононейропатия) или полифокальная (краниальная, проксимальная моторная, мононейропатия конечностей и туловища).
II. Автономная (вегетативная) нейропатия:
Кардиоваскулярная (ортостатическая гипотензия, синдром сердечной денервации);
Гастроинтестинальная (атония желудка, дискинезия желчных путей, диабетическая энтеропатия);
Урогенитальная (с нарушением функций мочевого пузыря и половой функции);
Нарушение у пациента способности распознавать гипогликемию;
Нарушение функции зрачка;
Нарушение функций потовых желез (дистальный ангидроз, гипергидроз при еде).
Табл. 7.20. Диабетическая нейропатия
 Этиология и патогенез
Этиология и патогенез
Основной причиной ДНЕ является гипергликемия. Предполагается несколько механизмов ее патогенеза:
Активизация полиолового пути метаболизма глюкозы, в результате чего в нервных клетках происходит накопление сорбитола, фруктозы и снижение содержания миоинозитола и глутатиона. Это, в свою очередь, приводит к активизации свободнорадикальных процессов и снижению уровня оксида азота;
Неэнзиматическое гликозилирование мембранных и цитоплазматических белков нервных клеток;
Микроангиопатия vasa nervorum, которая приводит к замедлению капиллярного кровотока и гипоксии нервов.
Эпидемиология
Распространенность ДНЕ при обоих типах СД составляет около 30 %. При СД-1 спустя 5 лет от начала заболевания она начинает выявляться у 10 % пациентов. Частота новых случаев ДНЕ при СД-2 составляет около 6 % пациентов в год. Наиболее частым вариантом является дистальная симметричная сенсомоторная ДНЕ.
Клинические проявления
Сенсомоторная ДНЕ проявляется комплексом двигательных и чувствительных нарушений. Частым симптомом дистальной формы ДНЕ являются парестезии, которые проявляются ощущением «ползания мурашек», онемением. Пациенты часто жалуются на зябкость ног, хотя они остаются теплыми на ощупь, что является признаком, позволяющим отличить полинейропатию от ишемических изменений, когда ноги на ощупь холодные. Ранним проявлением сенсорной нейропатии является нарушение вибрационной чувствительности. Характерным является синдром «беспокойных ног», представляющий собой сочетание ночных парестезии и повышенной чувствительности. Боли в ногах чаще беспокоят ночью, при этом иногда пациент не может выносить прикосновения одеяла. В типичном случае боли в противоположность таковым при облитерирующих заболеваниях артерий могут уменьшаться при ходьбе. Спустя годы боль может спонтанно прекратиться вследствие гибели мелких нервных волокон, отвечающих за болевую чувствительность. Гипоэстезия проявляется выпадением чувствительности по типу «чулок» и «перчаток». Нарушение глубокой, проприоцептивной чувствительности приводит к нарушению координации и затруднению передвижений (сенсорная атаксия). Пациент жалуется на «чужие ноги», ощущение «стояния на вате». Нарушение трофической иннервации приводит к дегенеративным изменениям кожи, костей и сухожилий. Нарушение болевой чувствительности приводит к частым, не замечаемым пациентом микротравмам стоп, которые легко инфицируются. Нарушение координации и ходьбы приводит к нефизиологическому перераспределению нагрузки на суставы стопы. В результате нарушаются анатомические взаимоотношения в опорно-двигательном аппарате ноги.
Деформируется свод стопы, развиваются отечность, фрактуры, хронические гнойные процессы (см. п. 7.8.5).
Выделяют несколько форм автономной ДНЕ. Причина кардиоваскулярной формы - нарушение иннервации сердечно-легочного комплекса и крупных сосудов. Блуждающий нерв является наиболее длинным нервом, в связи с чем поражается раньше других. В результате преобладания симпатических влияний развивается тахикардия покоя. Неадекватная реакция на ортостаз проявляется ортостатической гипотензией и синкопальными состояниями. Вегетативная денервация легочно-сердечного комплекса приводит к отсутствию вариабельности сердечного ритма. С автономной нейропатией связывают повышенную распространенность среди больных СД безболевых инфарктов миокарда.
Симптомами гастроинтестинальной формы ДНЕ являются гастропарез с замедленным или, наоборот, быстрым опорожнением желудка, что может создать сложности в подборе инсулинотерапии, поскольку время и объем всасывания углеводов неопределенно варьируют; атония пищевода, рефлюкс-эзофагит, дисфагия; водянистая диарея. Для урогенитальной формы ДНЕ характерны атония мочеточников и мочевого пузыря, приводящая к склонности к мочевым инфекциям; эректильная дисфункция (около 50 % больных СД); ретроградная эякуляция.
Другие возможные проявления вегетативной ДНЕ - нарушение способности распознавать гипогликемию, нарушение функции зрачка, нарушение функции потовых желез (ангидроз), диабетическая амиотрофия.
Диагностика
Неврологическое обследование пациентов с СД необходимо проводить ежегодно. Как минимум оно подразумевает проведение тестов, направленных на выявление дистальной сенсомоторной нейропатии. Для этого используется оценка вибрационной чувствительности при помощи градуированного камертона, тактильной чувствительности при помощи монофиламента, а также температурной и болевой чувствительности. По показаниям изучается состояние вегетативной нервной системы: для диагностики недостаточности парасимпатической иннервации сердца используют ряд функциональных проб, таких как измерение ЧСС при глубоком дыхании с оценкой вариабельности
сердечного ритма и пробу Вальсальвы; для диагностики недостаточности симпатической иннервации сердца используют ортостатическую пробу.
Дифференциальная диагностика
Нейропатии другого генеза (алкогольная, уремическая, при В 12 -дефицитной анемии и др.). Диагноз дисфункции того или иного органа в результате вегетативной нейропатии устанавливается только после исключения органной патологии.
Лечение
1. Оптимизация сахароснижающей терапии.
2. Уход за ногами (см. п. 7.8.5).
3. Эффективность нейротропных препаратов (α-липоевая кислота) подтверждается не во всех исследованиях.
4. Симптоматическая терапия (обезболивание, силденафил при эректильной дисфункции, флудрокортизон при ортостатической гипотонии и др.).
Прогноз
На начальных стадиях ДНЕ может быть обратимой на фоне стойкой компенсации СД. ДНЕ определяется у 80 % пациентов с язвенным поражением и является основным фактором риска ампутации ног
7.8.5. Синдром диабетической стопы
Синдром диабетической стопы (СДС) - патологическое состояние стопы при СД, возникающее на фоне поражения периферических нервов, кожи и мягких тканей, костей и суставов и проявляющееся острыми и хроническими язвами, костно-суставными поражениями и гнойнонекротическими процессами (табл. 7.21).
Этиология и патогенез
Патогенез СДС многокомпонентен и представлен сочетанием нейропатических и перфузионных нарушений с выраженной склонностью к инфицированию. Исходя из преобладания в патогенезе того или иного из перечисленных факторов, выделяют 3 основные формы
Табл. 7.21. Синдром диабетической стопы
 I. Нейропатическая форма
(60-70 %):
I. Нейропатическая форма
(60-70 %):
Без остеоартропатии;
С диабетической остеоартропатией.
II. Нейроишемическая (смешанная) форма (15-20 %).
III. Ишемическая форма (3-7 %).
Нейропатическая форма СДС. При диабетической нейропатии в первую очередь поражаются дистальные отделы наиболее длинных нервов. Длительный дефицит трофической импульсации приводит к гипотрофии кожи, костей, связок, сухожилий и мышц. Результатом гипотрофии соединительных структур является деформация стопы с нефизиологичным перераспределением опорной нагрузки и ее чрезмерным увеличением на отдельные участки. В этих местах, например в области проекции головок плюсневых костей, отмечаются утолщение кожи и формирование гиперкератозов. Постоянное давление на эти участки приводит к воспалительному аутолизу подлежащих мягких тканей, что создает предпосылки для формирования язвенного дефекта. В результате атрофии и нарушения потоотделения кожа становится сухой, легко трескается. Из-за снижения болевой чувствительности пациент часто не обращает внимания на происходящие изменения. Он не может своевременно обнаружить неудобство обуви, что приводит к образованию потертостей и мозолей, не замечает внедрения инородных тел, мелких ранок в местах растрескивания. Ситуацию усугубляет нарушение глубокой чувствительности, проявляющееся в нарушении походки, неправильной установке ноги. Наиболее часто язвенный дефект инфицируется стафилококками, стрептококками, бактериями кишечной группы; нередко присоединяется анаэробная флора. Нейропатическая остеоартропатия является результатом выраженных дистрофических изменений в костносуставном аппарате стопы (остеопороз, остеолиз, гиперостоз).
Ишемическая форма СДС является следствием атеросклероза артерий нижних конечностей, приводящего к нарушению магистрального кровотока, т.е. является одним из вариантов диабетической макроангиопатии.
Эпидемиология
СДС наблюдается у 10-25 %, а по некоторым данным, в той или иной форме у 30-80 % больных СД. В США ежегодные расходы на лечение больных с СД c СДС составляют 1 млрд. долларов.
Клинические проявления
При нейропатической форме СДС выделяют два наиболее частых вида поражения: нейропатическая язва и остеоартропатия (с развитием
 Рис. 7.12.
Нейропатическая язва при синдроме диабетической стопы
Рис. 7.12.
Нейропатическая язва при синдроме диабетической стопы
 Рис. 7.13.
Сустав Шарко при синдроме диабетической стопы
Рис. 7.13.
Сустав Шарко при синдроме диабетической стопы
сустава Шарко). Нейропатические язвы, как правило, локализуются в области подошвы и межпальцевых промежутков, т.е. на участках стопы, испытывающих наибольшее давление (рис. 7.12).
Деструктивные изменения костно-связочного аппарата стопы могут прогрессировать на протяжении многих месяцев и привести к выраженной костной деформации - диабетической остео-артропатии и формированию сустава Шарко, при этом стопу образно сравнивают с «мешком с костями»
При ишемической форме СДС
кожа на стопах холодная, бледная или цианотичная; реже имеет розовато-красный оттенок изза расширения поверхностных капилляров в ответ на ишемию. Язвенные дефекты возникают по типу акральных некрозов - на кончиках пальцев, краевой поверхности пяток (рис. 7.14).
Пульс на артериях стопы, подколенных и бедренных артериях ослаблен или не пальпируется.
В типичных случаях пациенты предъявляют жалобы на «перемежающуюся хромоту». Тяжесть ишемического поражения конечности определяется тремя основными факторами: тяжестью стеноза, развитием коллатерального кровотока, состоянием свертывающей системы крови.
Диагностика
Осмотр ног больного СД должен производиться каждый раз во время визита к врачу, не реже раза в полгода. Диагностика СДС включает:
 Рис. 7.14.
Акральные некрозы при ишемической форме синдрома диабетической стопы
Рис. 7.14.
Акральные некрозы при ишемической форме синдрома диабетической стопы
Осмотр ног;
Оценку неврологического статуса - различных видов чувствительности, сухожильных рефлексов, электромиографию;
Оценку состояния артериального кровотока - ангиографию, доплерометрию, доплерографию;
Рентгенографию стоп и голеностопных суставов;
Бактериологическое исследование раневого отделяемого.
Дифференциальная диагностика
Проводится с раневыми процессами на стопах другого генеза, а также другими окклюзионными заболеваниями сосудов нижних конечностей и патологией суставов стопы. Кроме того, необходимо дифференцировать клинические формы СДС (табл. 7.22).
Лечение
Лечение нейропатически-инфицированной формы СДС включает комплекс следующих мероприятий:
Оптимизацию компенсации СД, как правило, увеличение дозы инсулина, а при СД-2 - перевод на него;
Системную антибиотикотерапию;
Полную разгрузку стопы (это может в течение нескольких недель привести к заживлению язв, существующих годами);
Местную обработку раны с удалением участков гиперкератоза;
Уход за ногами, правильный подбор и ношение специальной обуви. Своевременно проводенная консервативная терапия позволяет
избежать оперативного вмешательства в 95 % случаев.
Табл. 7.22. Дифференциальная диагностика клинических форм СДС
 Лечение ишемической
формы СДС включает:
Лечение ишемической
формы СДС включает:
Оптимизацию компенсации СД, как правило, увеличение дозы инсулина, а при СД-2 - перевод на него;
При отсутствии язвенно-некротических поражений эрготерапию (1-2-часовая ходьба в день, способствующая развитию коллатерального кровотока);
Реваскуляризационные операции на пораженных сосудах;
Консервативную терапию: антикоагулянты, аспирин (до 100 мг/сут), при необходимости - фибринолитики, препараты простагландина E1 и простациклина.
При развитии обширного гнойно-некротического поражения при всех вариантах СДС ставится вопрос об ампутации.
Прогноз
От 50 до 70 % от общего количества выполненных ампутаций ног приходится на долю больных СД. Ампутация ног у пациентов с СД производятся в 20-40 раз чаще, чем у лиц без диабета.
7.9. САХАРНЫЙ ДИАБЕТ И БЕРЕМЕННОСТЬ
Гестационный сахарный диабет (ГСД) - это нарушение толерантности к глюкозе, впервые выявленное во время беременности (табл. 7.23). Это определение не исключает того, что патология углеводного обмена могла предшествовать наступлению беременности. ГСД следует отличать от ситуаций, когда у женщины с диагностированным ранее диабетом (в силу возраста, чаще СД-1) наступает беременность.
Этиология и патогенез
При ГСД сходны с таковыми при СД-2. Высокий уровень овариальных и плацентарных стероидов, а также увеличение образования кортизола корой надпочечников приводят при беременности к развитию физиологической инсулинорезистентности. Развитие ГСД связывают с тем, что инсулинорезистентность, закономерно развивающаяся при беременности, и, следовательно, повышенная потребность в инсулине у предрасположенных лиц превышает функциональную способность β-клеток ПЖЖ. После родов с возвращением гормональных и метаболических взаимоотношений к исходному уровню он, как правило, проходит.
Табл. 7.23. Гестационный сахарный диабет
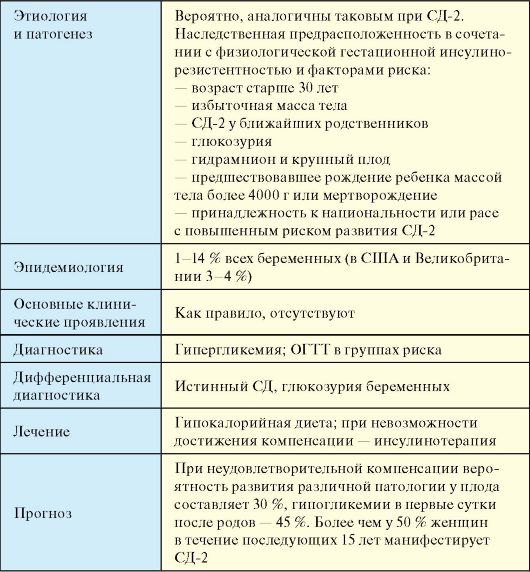 ГСД
обычно развивается в середине 2 триместр, между 4 и 8 месяцами
беременности. Подавляющее большинство пациенток имеет избыток массы тела
и отягощенный по СД-2 анамнез. Факторы риска развития ГСД, а также
группы женщин с низким риском развития ГСД приведены в табл. 7.24.
ГСД
обычно развивается в середине 2 триместр, между 4 и 8 месяцами
беременности. Подавляющее большинство пациенток имеет избыток массы тела
и отягощенный по СД-2 анамнез. Факторы риска развития ГСД, а также
группы женщин с низким риском развития ГСД приведены в табл. 7.24.
Табл. 7.24. Факторы риска развития гестационного сахарного диабета
 Гипергликемия
матери приводит к гипергликемии в системе кровообращения ребенка.
Глюкоза легко проникает через плаценту и непрерывно переходит к плоду из
крови матери. Также происходят активный транспорт аминокислот и перенос
кетоновых тел плоду. В отличие от этого инсулин, глюкагон и свободные
жирные кислоты матери в кровь плода не попадают. В первые 9-12 недель
беременности ПЖЖ плода еще не вырабатывает собственный инсулин. Это
время соответствует той фазе органогенеза плода, когда при постоянной
гипергликемии у матери могут формироваться различные пороки развития
(сердца, позвоночника, спинного мозга, ЖКТ). С 12-й недели беременности
ПЖЖ плода начинает синтезировать инсулин, и в ответ на гипергликемию
развиваются реактивная гипертрофия и гиперплазия β-клеток фетальной ПЖЖ.
Вследствие гиперинсулинемии развиваются макросомия плода, а также
угнетение синтеза лецитина, что объясняет высокую частоту развития
респираторного дистресссиндрома у новорожденных. В результате
гиперплазии β-клеток и гиперинсулинемии появляется склонность к тяжелым и
длительным гипогликемиям.
Гипергликемия
матери приводит к гипергликемии в системе кровообращения ребенка.
Глюкоза легко проникает через плаценту и непрерывно переходит к плоду из
крови матери. Также происходят активный транспорт аминокислот и перенос
кетоновых тел плоду. В отличие от этого инсулин, глюкагон и свободные
жирные кислоты матери в кровь плода не попадают. В первые 9-12 недель
беременности ПЖЖ плода еще не вырабатывает собственный инсулин. Это
время соответствует той фазе органогенеза плода, когда при постоянной
гипергликемии у матери могут формироваться различные пороки развития
(сердца, позвоночника, спинного мозга, ЖКТ). С 12-й недели беременности
ПЖЖ плода начинает синтезировать инсулин, и в ответ на гипергликемию
развиваются реактивная гипертрофия и гиперплазия β-клеток фетальной ПЖЖ.
Вследствие гиперинсулинемии развиваются макросомия плода, а также
угнетение синтеза лецитина, что объясняет высокую частоту развития
респираторного дистресссиндрома у новорожденных. В результате
гиперплазии β-клеток и гиперинсулинемии появляется склонность к тяжелым и
длительным гипогликемиям.
Эпидемиология
СД страдают 0,3 % всех женщин репродуктивного возраста, 0,2-0,3 % беременных уже исходно больны СД, а в 1-14 % беременностей развивается ГСД или манифестирует истинный СД. Распространенность ГСД варьирует в разных популяциях, так, в США он выявляется примерно у 4 % беременных (135 тыс. случаев в год).
Клинические проявления
При ГСД отсутствуют. Могут быть неспецифические симптомы декомпенсации СД.
Диагностика
Определение уровня глюкозы крови натощак показано всем беременным женщинам в рамках биохимического анализа крови. Женщинам, которые относятся к группе риска (табл. 7.24), показано проведение орального глюкозотолерантного теста (ОГТТ). Описано много вариантов его проведения у беременных. Наиболее простой из них подразумевает следующие правила:
3 дня до обследования женщина находится на обычном питании и придерживается обычной для себя физической активности;
Тест проводится утром натощак, после ночного голодания не менее 8 часов;
После взятия пробы крови натощак женщина в течение 5 минут выпивает раствор, состоящий из 75 грамм сухой глюкозы, растворенной в 250-300 мл воды; повторное определение уровня гликемии проводится через 2 часа.
Диагноз ГСД устанавливается по следующим критериям:
Глюкоза цельной крови (венозной, капиллярной) натощак > 6,1 ммоль/л или
Глюкоза плазмы венозной крови ≥ 7 ммоль/л или
Глюкоза цельной капиллярной крови или плазмы венозной крови через 2 часа после нагрузки 75 г глюкозы ≥ 7,8 ммоль/л.
Если у женщины, которая относится к группе риска, результаты исследования соответствуют норме, тест проводится повторно на 24-28 неделе беременности.
Дифференциальная диагностика
ГСД и истинный СД; глюкозурия беременных.
Лечение
Риск для матери и плода, а также подходы к лечению СД и особенности контроля за ним при ГСД и при истинном СД одинаковы. Поздние осложнения СД во время беременности могут значительно прогрессировать, однако при качественной компенсации СД показаний для прерывания беременности нет. Женщина, страдающая СД (как правило, речь идет о СД-1), должна планировать беременность в молодом возрасте, когда риск развития осложнений наиболее низок. Если планируется беременность, то рекомендуется отменять конт-
рацепцию спустя несколько месяцев после достижения оптимальной компенсации. Противопоказаниями к планированию беременности являются тяжелая нефропатия с прогрессирующей почечной недостаточностью, тяжелая ИБС, тяжелая пролиферативная ретинопатия, не поддающаяся коррекции, кетоацидоз на ранних сроках беременности (кетоновые тела являются тератогенными факторами).
Целью лечения ГСД и истинного СД во время беременности является достижение следующих лабораторных показателей:
Гликемия натощак < 5-5,8 ммоль/л;
Гликемия через 1 ч после еды < 7,8 ммоль/л;
Гликемия через 2 ч после еды < 6,7 ммоль/л;
Среднее значение дневного гликемического профиля < 5,5 ммоль/л;
Уровень HbA1c при ежемесячном контроле, как у здоровых (4-6 %).
При СД-1, как и вне беременности, женщина должна получать интенсивную инсулинотерапию, однако уровень гликемии во время беременности рекомендуется оценивать 7-8 раз в сутки. При невозможности достижения нормогликемической компенсации на фоне обычных инъекций, необходимо рассмотреть вопрос о переводе пациентки на инсулинотерапию при помощи дозатора инсулина.
На первым этапе лечения ГСД назначается диетотерапия, заключающаяся в ограничении суточного калоража примерно до 25 кКал/кг фактического веса, в первую очередь за счет легкоусваиваемых углеводов и жиров животного происхождения, а также расширение физических нагрузок. Если на фоне диетотерапии не удается достичь поставленных целей лечения, пациентке необходимо назначить интенсивную инсулинотерапию. Любые таблетированные сахароснижающие препараты (ТСП) при беременности противопоказаны. На инсулинотерапию оказывается необходимым переводить около 15 % женщин.
Прогноз
При неудовлетворительной компенсации ГСД и СД во время беременности вероятность развития различной патологии у плода составляет 30 % (риск в 12 раз выше, чем в общей популяции). Более чем у 50 % женщин, у которых во время беременности выявлялся ГСД, в течение последующих 15 лет манифестирует СД-2.
Как и любое другое серьезное заболевание, в значительной мере влияет на организм человека.
При развитии сахарного диабета наблюдаются не только гормональные изменения, но и патологические процессы, влияющие на различные внутренние органы и группы органов.
За изучение анатомических особенностей организма пациентов, страдающих сахарным диабетом, отвечает раздел медицины под названием патологическая анатомия. Чем же отличается сопровождающая сахарный диабет патанатомия?
Патологическая анатомия: что это?
Внутреннее устройство человека, а также особенности строения и развития его органов изучаются морфологией человека.
Нехарактерные для здорового человека изменения органов, возникающие вследствие развития того или иного заболевания являются предметом исследования патологической анатомии.
Особенности влияния той или иной патологии на человека являются важнейшими данными, помогающими разработать и внедрить правильное лечение. Особенно важно понимать механизм воздействия заболевания для понимания причин возникновения того или иного недуга.
Правильность оказания симптоматической помощи, которая в определенных случаях до сих пор остается единственным средством спасения жизни пациента, также в значительной мере зависит от знаний, полученных с помощью патанатомии. Поэтому вскрытие и исследование тел, а также всестороннее изучение хирургического материала являются одним из основных путей развития медицины.
Паталогоанатомия – важный метод обучения новых медицинских кадров.
Панатомия сахарного диабета: общая характеристика
 Изучением анатомии пациентов с диабетом занимается подраздел медицины под названием патанатомия эндокринной системы.
Изучением анатомии пациентов с диабетом занимается подраздел медицины под названием патанатомия эндокринной системы.
При этом более характерны не макро-поражения, вызывающие кардиосклероз и , а микроангиопатия, когда дегенеративные процессы протекают в капиллярах. При этом возможно возникновение таких патологий, как , поражение капилляров почек и .
Видимое нарушение морфологии свидетельствует о длительном течении болезни.
При длительном и интенсивном развитии диабета выявляется нарушение морфологии внутренних органов, прежде всего – поджелудочной железы. Изменения дистрофического или атрофического характера могут быть выявлены также и в других железах и органах, в том числе и относящихся к ЦНС.
Классификация
Заболевание принято разделять на 4 различные , в зависимости от предполагаемого происхождения заболевания.
Этиологические формы диабета:
Разберем характеристики каждой из форм данного эндокринного заболевания. Для первого типа характерна абсолютная деструкция особых клеток железы, способных к продуцированию инсулина.
В результате производство этого жизненно важного гормона прекращается полностью, и у человека отсутствует возможность транспортировать глюкозу непосредственно в клетки организма. Второй тип характеризуется развитием у пациента нечувствительности к инсулину.
Таким образом, необходимо наличие в крови нормального или даже повышенного количества данного гормона – синтезированного поджелудочной железой или даже поступающего извне с . Данная патология инсулиновых рецепторов обычно развивается на фоне .
 Гестационная форма известна как «диабет беременных». Он характеризуется нарушением глюкозной толерантности, которая возникла в период беременности, и значительной .
Гестационная форма известна как «диабет беременных». Он характеризуется нарушением глюкозной толерантности, которая возникла в период беременности, и значительной .
После родов состояние организма обычно нормализуется без влияния извне.
Латентный диабет – это, по сути, организма. Оно характеризуется очень медленным развитием инсулиновой резистентности и достаточно долгое время протекает без ощутимых симптомов. Определить это состояние, которое многие врачи считают стадией заболевания, можно только с помощью нескольких анализов на уровень глюкозы.
Если данный показатель крови достигает 120 мг, и результат удерживается стойко – есть повод говорить о преддиабете. Говорят также и о . Манифестация – это первое клиническое проявление диабета.
Манифестация говорит о значительном развитии заболевания.
Не стоит путать это состояние и начало заболевания, ведь значительное снижение резистентности инсулиновых рецепторов достаточно длительное время может протекать без каких-либо симптомов.
Морфологические признаки и проявления патологии
При развитии заболевания происходит постепенное накопление амилоида в поджелудочной железе . В случае запущенного диабета наблюдается даже полное замещение амилоидными образованиями островков Лангерганса.
В некоторых случаях наблюдается фиброз поджелудочной железы, когда инсулиновые бугорки замещаются нефункциональной соединительной тканью.

Стадии развития атеросклероза сосудов
Описанные выше патологии капилляров приводят со временем к более серьезным нарушениям функциональности кровеносной системы. Так, выраженный атеросклероз является одним из следствий развития заболевания.
Не являясь специфическим недугом, у диабетиков он начинается раньше и прогрессирует значительно быстрее, поражая в основном крупные кровеносные сосуды.
Диабетические осложнения
 Помимо и сосудами, развиваются и другие осложнения этого заболевания – острые, поздние и хронические.
Помимо и сосудами, развиваются и другие осложнения этого заболевания – острые, поздние и хронические.
К острым относится накопление в крови продуктов метаболизма и кетоновых тел, приводящее к нарушениям работы органов – .
Видео по теме
О причинах возникновения и способах лечения диабета в видео:
В большинстве случаев такая опасная патология поджелудочной железы оставляет на этом органе заметный морфологический след, изучение которого помогает лучше понять природу болезни и методы ее лечения.









